Hvilket ville have de største kohæsionskræfter mellem dets molekyler vand eller olie?
Kohæsionskræfterne mellem vandmolekyler er stærkere end kohæsionskræfterne mellem oliemolekyler, fordi vandmolekyler er polære, hvilket betyder, at de har en positiv ende og en negativ ende. Denne polaritet gør det muligt for vandmolekyler at danne brintbindinger med hinanden, som er stærke intermolekylære kræfter. Oliemolekyler er på den anden side upolære, hvilket betyder, at de ikke har en positiv eller negativ ende. Det betyder, at oliemolekyler ikke kan danne brintbindinger med hinanden, og de eneste kræfter, der holder dem sammen, er svage van der Waals-kræfter. Derfor har vand stærkere kohæsionskræfter mellem sine molekyler end olie.
Sidste artikelHvad bestemmer forholdet mellem ioner i en ionforbindelse?
Næste artikelHvad er ammoniakens ka?
 Varme artikler
Varme artikler
-
 Røntgenbilleder viser, hvordan perioder med stress ændrede en istidshyæne til knoglenPalæontologen Jennifer Anné efterforsker en plettet hyæne. Forskerne brugte knogler fra disse moderne dyr som analoger for bedre at forstå 40, 000 år gamle hulehyænefossiler fra istiden. Kredit:Childr
Røntgenbilleder viser, hvordan perioder med stress ændrede en istidshyæne til knoglenPalæontologen Jennifer Anné efterforsker en plettet hyæne. Forskerne brugte knogler fra disse moderne dyr som analoger for bedre at forstå 40, 000 år gamle hulehyænefossiler fra istiden. Kredit:Childr -
 Forskere udvikler et materiale til brug i strålingstolerante enhederCH3NH3PbBr3 (MAPbBr3) monokrystalbilleddannelse under UV-lys og under synligt omgivende lys. Kredit:Arthur Ishteev Russiske videnskabsmænd har udviklet et unikt materiale baseret på halogenidperovs
Forskere udvikler et materiale til brug i strålingstolerante enhederCH3NH3PbBr3 (MAPbBr3) monokrystalbilleddannelse under UV-lys og under synligt omgivende lys. Kredit:Arthur Ishteev Russiske videnskabsmænd har udviklet et unikt materiale baseret på halogenidperovs -
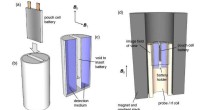 Kemikere udvikler MRI-lignende teknik til at opdage, hvad der fejler batterierEt team af kemikere har udviklet en MRI-baseret teknik, der hurtigt kan diagnosticere, hvad der fejler visse typer batterier - fra at bestemme, hvor meget ladning der er tilbage til at opdage interne
Kemikere udvikler MRI-lignende teknik til at opdage, hvad der fejler batterierEt team af kemikere har udviklet en MRI-baseret teknik, der hurtigt kan diagnosticere, hvad der fejler visse typer batterier - fra at bestemme, hvor meget ladning der er tilbage til at opdage interne -
 Lysaktiveret metalkatalysator ødelægger kræftcellernes vitale energikildeKredit:University of Warwick Et metal i en rumalder, der var en del af asteroiden, der ødelagde dinosaurerne, kunne give en ny metode til selektiv behandling af kræfttumorer ved hjælp af lys. For
Lysaktiveret metalkatalysator ødelægger kræftcellernes vitale energikildeKredit:University of Warwick Et metal i en rumalder, der var en del af asteroiden, der ødelagde dinosaurerne, kunne give en ny metode til selektiv behandling af kræfttumorer ved hjælp af lys. For
- Dette enkle matematikbegreb former folketællingen i 2020 - og dine offentlige tjenester
- Sådan beregnes apotemet til en polygon
- Spatiotemporale variationer af regntidens nedbør i det tibetanske plateau i løbet af de sidste to …
- Samarbejde giver lovende materiale til kvanteberegning
- Brug af økonometri til at definere effektive COVID-19 lockdown-strategier
- Undersøgelse med 950 ledere fra en offentlig institution undersøger hyppighed og årsager til defe…


