Hvad er reaktionen af sølvnitrat?
* Reaktion med halogenider: Sølvnitrat reagerer med halogenider og danner uopløselige sølvhalogenider. Denne reaktion bruges i den kvalitative analyse af halogenider.
$$AgNO_3 + NaCl \rightarrow AgCl + NaNO_3$$
* Reaktion med sulfider: Sølvnitrat reagerer med sulfider og danner uopløseligt sølvsulfid. Denne reaktion bruges i den kvalitative analyse af sulfider.
$$AgNO_3 + Na_2S \rightarrow Ag_2S + 2NaNO_3$$
* Reaktion med karbonater: Sølvnitrat reagerer med carbonater og danner uopløseligt sølvcarbonat. Denne reaktion bruges i den kvalitative analyse af carbonater.
$$AgNO_3 + Na_2CO_3 \rightarrow Ag_2CO_3 + 2NaNO_3$$
* Reaktion med fosfater: Sølvnitrat reagerer med fosfater og danner uopløseligt sølvfosfat. Denne reaktion bruges i den kvalitative analyse af fosfater.
$$AgNO_3 + Na_3PO_4 \rightarrow Ag_3PO_4 + 3NaNO_3$$
* Reaktion med proteiner: Sølvnitrat reagerer med proteiner og danner uopløseligt sølvproteinat. Denne reaktion bruges i den kvalitative analyse af proteiner.
$$AgNO_3 + albumin \rightarrow Ag-albumin + HNO_3$$
* Reaktion med ammoniak: Sølvnitrat reagerer med ammoniak og danner en kompleks ion, [Ag(NH_3)_2]^+). Denne reaktion anvendes til fremstilling af sølvdiaminkomplekser.
$$AgNO_3 + 2NH_3 \rightarrow [Ag(NH_3)_2]NO_3$$
* Reaktion med thiosulfat: Sølvnitrat reagerer med thiosulfat og danner en kompleks ion, [Ag(S_2O_3)_2]^{3-). Denne reaktion anvendes til den argentometriske titrering af thiosulfat.
$$AgNO_3 + 2S_2O_3^{2-} \rightarrow [Ag(S_2O_3)_2]^{3-} + NO_3^-$$
* Reaktion med cyanid: Sølvnitrat reagerer med cyanid og danner en kompleks ion, [Ag(CN)_2]^{-). Denne reaktion bruges i den kvalitative analyse af cyanid.
$$AgNO_3 + 2CN^- \rightarrow [Ag(CN)_2]^- + NO_3^-$$
* Reaktion med iodid: Sølvnitrat reagerer med iodid og danner uopløseligt sølviodid. Denne reaktion bruges i den kvalitative analyse af iodid.
$$AgNO_3 + KI \rightarrow AgI + KNO_3$$
Sidste artikelHvad er oxidationstallet for O i ClO4-is?
Næste artikelEr grundstoffet plutonium menneskeskabt?
 Varme artikler
Varme artikler
-
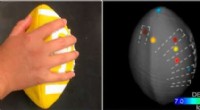 Robotics tager massespecifikationer til den tredje dimension for retsmedicin, farma applikationerVed at kombinere en robotarm og massespektrometri, forskere kan analysere overfladen af 3D-objekter, såsom fodbolde. Kredit:American Chemical Society Inden for det seneste årti, der er gjort man
Robotics tager massespecifikationer til den tredje dimension for retsmedicin, farma applikationerVed at kombinere en robotarm og massespektrometri, forskere kan analysere overfladen af 3D-objekter, såsom fodbolde. Kredit:American Chemical Society Inden for det seneste årti, der er gjort man -
 Forskere afslører en køreplan for at hjælpe med udvikling af osteoporosebehandlingFra venstre mod højre:forskningsassistent Ruben Garcia-Ordonez, Forskningsassistent Jie Zheng, Professor Pat Griffin, Forskningsassistent Scott Novick, Stabsforsker Mi Ra Chang. Kredit:Scripps Researc
Forskere afslører en køreplan for at hjælpe med udvikling af osteoporosebehandlingFra venstre mod højre:forskningsassistent Ruben Garcia-Ordonez, Forskningsassistent Jie Zheng, Professor Pat Griffin, Forskningsassistent Scott Novick, Stabsforsker Mi Ra Chang. Kredit:Scripps Researc -
 Fremstilling af mekanisk hudFlydende metalkompositter muliggør blød, strækbare kredsløb, der er elektrisk ledende, mekanisk selvhelbredende, og meget tilpasningsdygtig. Kredit:Soft Machines Lab, Carnegie Mellon University Bl
Fremstilling af mekanisk hudFlydende metalkompositter muliggør blød, strækbare kredsløb, der er elektrisk ledende, mekanisk selvhelbredende, og meget tilpasningsdygtig. Kredit:Soft Machines Lab, Carnegie Mellon University Bl -
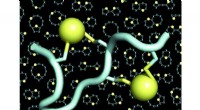 Dobbeltbroede peptider binder ethvert sygdomsmålEn model af et dobbeltbrokoblet peptid (peptidet i lyseblåt, de to broer i gult). Baggrunden for figurerne viser mange eksempler på skeletter (også kaldet stilladser eller rygrade) af dobbeltbroforbun
Dobbeltbroede peptider binder ethvert sygdomsmålEn model af et dobbeltbrokoblet peptid (peptidet i lyseblåt, de to broer i gult). Baggrunden for figurerne viser mange eksempler på skeletter (også kaldet stilladser eller rygrade) af dobbeltbroforbun
- Rekordstor britisk nedbør i vinteren 2013-14 forårsaget af troperne, stratosfæren og klimaopvarmn…
- Optisk interferometri visualiserer, hvor ofte liljer udsender flygtige organiske forbindelser
- Kinas bilsalg synker med 48,4% i marts, da virus skader efterspørgslen
- Hvordan vi passer på miljøet kan have sociale konsekvenser
- Spildte fuglefjer blev til mad
- Farlige sneakerbølger puslespil videnskabsmænd


