Hvor mange gram vandfri nikkel 2-sulfat fremstilles af 8.753 heptahydrat?
Den molære masse af NiSO4 er 154,75 g/mol, mens den molære masse af NiSO4·7H2O er 280,86 g/mol.
Den kemiske ligning for omdannelsen af NiSO4·7H2O til vandfri NiSO4 er:
NiSO4·7H2O → NiSO4 + 7H2O
Ud fra denne ligning kan vi se, at et mol NiSO4·7H2O producerer et mol NiSO4.
For at beregne antallet af mol NiSO4·7H2O i 8,753 g, dividerer vi massen med dens molære masse:
Mol NiSO4·7H2O =8,753 g / 280,86 g/mol =0,0312 mol
Da et mol NiSO4·7H2O producerer et mol NiSO4, ved vi, at der vil blive produceret 0,0312 mol NiSO4.
Nu kan vi beregne massen af vandfri NiSO4 produceret ved at gange molerne med dens molære masse:
Masse af NiSO4 =0,0312 mol * 154,75 g/mol =4,838 g
Derfor vil 8,753 gram nikkelsulfat-heptahydrat producere 4,838 gram vandfrit nikkel 2-sulfat.
Sidste artikelHvorfor viser furan ikke nukleofil substitutionsreaktion?
Næste artikelHvad er PH på 8,5?
 Varme artikler
Varme artikler
-
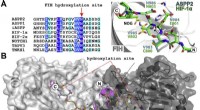 Hydroxyleringen af ASPP2 og andre ankyrin-gentagelsesdomæneproteinerUdsigter fra krystalstrukturer af FIH i kompleks med ASPP-afledte peptider. En (venstre) sekvensjustering af ASPP-proteiner med rapporterede FIH-substrater. (Højre) Overlejring af krystalstrukturafled
Hydroxyleringen af ASPP2 og andre ankyrin-gentagelsesdomæneproteinerUdsigter fra krystalstrukturer af FIH i kompleks med ASPP-afledte peptider. En (venstre) sekvensjustering af ASPP-proteiner med rapporterede FIH-substrater. (Højre) Overlejring af krystalstrukturafled -
 Dæmpning af havplastikKredit:CC0 Public Domain Efterhånden som mennesker i udviklingslandene bliver mere velhavende, de ender med at købe mere plastik. Men disse områder har ofte ikke gode affaldshåndteringsprocedurer
Dæmpning af havplastikKredit:CC0 Public Domain Efterhånden som mennesker i udviklingslandene bliver mere velhavende, de ender med at købe mere plastik. Men disse områder har ofte ikke gode affaldshåndteringsprocedurer -
 At lave molekyler, der glimterKuldioxid er en nyttig råstofgas til syntese af komplekse funktionelle materialer. Kredit:Supparsorn Wantarnagon / 123rf Forskere ved Singapores agentur for videnskab, Teknologi og forskning (A*ST
At lave molekyler, der glimterKuldioxid er en nyttig råstofgas til syntese af komplekse funktionelle materialer. Kredit:Supparsorn Wantarnagon / 123rf Forskere ved Singapores agentur for videnskab, Teknologi og forskning (A*ST -
 En fortælling om hyrder og spiralerKrigsskade med konsekvenser:efter Anden Verdenskrig, Giuseppe Torrettis marmorrelief Tilbedelse af hyrderne overlevede kun i fragmenter (brunlige sektioner), som er vist her i kombination med et sort
En fortælling om hyrder og spiralerKrigsskade med konsekvenser:efter Anden Verdenskrig, Giuseppe Torrettis marmorrelief Tilbedelse af hyrderne overlevede kun i fragmenter (brunlige sektioner), som er vist her i kombination med et sort
- Vandknapheds fodaftryk afslører virkningerne af individuelle kostvalg i USA
- Sort huls politi opdager et sovende sort hul uden for Mælkevejsgalaksen
- NASA opdager kortvarig tropisk cyklon Alfred
- Skosnorteori:Videnskaben viser, hvorfor snørebåndene bliver løst
- Sommerens skovbrande, du ikke hørte om, og de invasive arter, der driver dem
- Forskere opdager, hvordan nerveceller i flagermushjerner reagerer på deres miljø og sociale intera…


