Når der forekommer kemiske reaktioner, er atomer, der aldrig er ioniseret, omarrangeres ødelagt eller fordampet?
* atomer ødelægges eller fordampes: Dette skyldes lov om bevarelse af masse , der angiver, at der ikke kan skabes noget, der kan skabes eller ødelægges i almindelige kemiske reaktioner. Atomer ændrer simpelthen deres arrangement og binding til dannelse af nye molekyler.
* atomer kan ioniseres: Ionisering involverer forstærkning eller tab af elektroner med et atom, hvilket skaber en ladet art kaldet en ion. Mange kemiske reaktioner involverer dannelsen af ioner, især i opløsninger.
* atomer kan omarrangeres: Dette er kernen i kemiske reaktioner. Atomer er bundet sammen på forskellige måder at danne nye molekyler med forskellige egenskaber. Denne omarrangement kan involvere at bryde eksisterende obligationer og danne nye.
Eksempler:
* forbrænding: Ved forbrænding af træ kombineres kulstofatomerne i træ med iltatomer fra luften for at danne kuldioxid. Atomerne i sig selv ødelægges ikke, men de omarrangeres for at danne et nyt molekyle.
* Elektrolyse af vand: At passere elektricitet gennem vand får vandmolekylerne til at nedbrydes i brint og iltgas. Her ødelægges ikke brint- og iltatomerne, men omarrangeres og ioniseres.
Nøglepunkt: Mens atomer aldrig ødelægges eller fordampes i kemiske reaktioner, kan de ioniseres og deres arrangement inden for molekyler kan ændres drastisk.
Sidste artikelHvordan gælder loven om samtalemasse for kemiske reaktioner?
Næste artikelKan forbindelser skabes af kemiske reaktioner?
 Varme artikler
Varme artikler
-
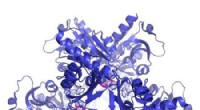 Ny tilgang gør det lettere at finde nye lægemidlerBåndrepræsentation af strukturen af et enzym kendt som ATP-PRT fra TB-bakterier (blå), bundet til en allosterisk aktivator (pink). Kredit:Luiz Carvalho Forskere har skabt en ny metode til screen
Ny tilgang gør det lettere at finde nye lægemidlerBåndrepræsentation af strukturen af et enzym kendt som ATP-PRT fra TB-bakterier (blå), bundet til en allosterisk aktivator (pink). Kredit:Luiz Carvalho Forskere har skabt en ny metode til screen -
 Det mest detaljerede røntgenbillede af batterier har endnu ikke afsløret, hvorfor de stadig ikke e…Dybdegående beregningsmodeller af kommercielle lithium-ion batterielektroder afslører specifikt, hvor der sker skade ved brug. Kredit:Purdue University billede/Kejie Zhao Elbiler er afhængige af d
Det mest detaljerede røntgenbillede af batterier har endnu ikke afsløret, hvorfor de stadig ikke e…Dybdegående beregningsmodeller af kommercielle lithium-ion batterielektroder afslører specifikt, hvor der sker skade ved brug. Kredit:Purdue University billede/Kejie Zhao Elbiler er afhængige af d -
 Ud af det blå:Middelalderfragmenter giver overraskelserEn bærbar-punkt røntgen-flourescens (p-XRF) scanner bruges på et belyst manuskriptfragment. Kredit:Cornell University Library Analyse af pigmenter i middelalderbelyste manuskriptsider ved Cornell
Ud af det blå:Middelalderfragmenter giver overraskelserEn bærbar-punkt røntgen-flourescens (p-XRF) scanner bruges på et belyst manuskriptfragment. Kredit:Cornell University Library Analyse af pigmenter i middelalderbelyste manuskriptsider ved Cornell -
 Opdagelse af bakteriel enzymaktivitet kan føre til nye sukkerbaserede lægemidlerKredit:Danmarks Tekniske Universitet Forskere fra DTU Biosustain og DTU Bioengineering har belyst aktiviteten af enzymet N-acetylgalactosaminidase (GH109), hvis aktivitetsmekanisme indtil nu har
Opdagelse af bakteriel enzymaktivitet kan føre til nye sukkerbaserede lægemidlerKredit:Danmarks Tekniske Universitet Forskere fra DTU Biosustain og DTU Bioengineering har belyst aktiviteten af enzymet N-acetylgalactosaminidase (GH109), hvis aktivitetsmekanisme indtil nu har
- Hvor mange kubik inches i en gård?
- Hvor godt du klarer dig i skolen afhænger af, hvor meget dine lærere ved:Indsigt fra 14 fransktale…
- Er der noget vand eller liv på kviksølv?
- Sulfid og jern arbejder sammen for at afsløre en ny vej til radionuklidsekvestering
- Solar Orbiter skal afsløre Suns hemmeligheder
- Hvorfor kulstofafgiften vil koste nogle Maritimes familier mere end andre


