Hvor mange mol gas optager 1,3 L ved et tryk 3,89 atmosfærer og temperatur 323 K?
1. Den ideelle gaslov
Den ideelle gaslov er repræsenteret af ligningen:
PV =NRT
Hvor:
* P =pres (i atmosfærer)
* V =volumen (i liter)
* n =antal mol
* R =ideel gaskonstant (0,0821 l · atm/mol · k)
* T =temperatur (i Kelvin)
2. Omarranger ligningen
Vi ønsker at løse for 'n' (antal mol), så vi omarrangerer ligningen:
n =pv / rt
3. Tilslut værdierne
* P =3,89 atm
* V =1,3 L
* R =0,0821 l · atm/mol · k
* T =323 K
4. Beregn
n =(3,89 atm * 1,3 l) / (0,0821 l · atm / mol · k * 323 K)
n ≈ 0,195 mol
Derfor besætter ca. 0,195 mol gas 1,3 L ved et tryk på 3,89 atmosfærer og en temperatur på 323 K.
 Varme artikler
Varme artikler
-
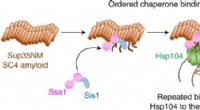 Tre ledsagere koordinerer opdelingen af amyloidfibriller i gærKredit:Yoshiko Nakagawa et al., Nature Chemical Biology (2022). DOI:10.1038/s41589-021-00951-y I et fund, der har vigtige konsekvenser for neurodegenerative lidelser såsom Alzheimers sygdom, har RI
Tre ledsagere koordinerer opdelingen af amyloidfibriller i gærKredit:Yoshiko Nakagawa et al., Nature Chemical Biology (2022). DOI:10.1038/s41589-021-00951-y I et fund, der har vigtige konsekvenser for neurodegenerative lidelser såsom Alzheimers sygdom, har RI -
 Sikring af broccolispirer bevarer deres kræftbekæmpende forbindelserKredit:CC0 Public Domain Rå broccolispirer, en rig kilde til potentielle kræftbekæmpende forbindelser, er blevet en populær helsekost i de seneste år. Men konventionel varmebehandling, der bruges
Sikring af broccolispirer bevarer deres kræftbekæmpende forbindelserKredit:CC0 Public Domain Rå broccolispirer, en rig kilde til potentielle kræftbekæmpende forbindelser, er blevet en populær helsekost i de seneste år. Men konventionel varmebehandling, der bruges -
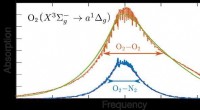 Forskere opdager, hvordan kolliderende iltmolekyler absorberer lysFigur:Eksperimentelle og teoretiske spektre for lysabsorption på grund af kollision af ilt (O2) molekyler med andre iltmolekyler og med nitrogen (N2) molekyler. Som vist her, absorptionen på grund af
Forskere opdager, hvordan kolliderende iltmolekyler absorberer lysFigur:Eksperimentelle og teoretiske spektre for lysabsorption på grund af kollision af ilt (O2) molekyler med andre iltmolekyler og med nitrogen (N2) molekyler. Som vist her, absorptionen på grund af -
 Lavpriskatalysator hjælper med at omdanne havvand til brændstof i stor skalaKredit:Pixabay/CC0 Public Domain Søværnets søgen efter at drive sine skibe ved at omdanne havvand til brændstof er et skridt nærmere. University of Rochester kemiingeniører, i samarbejde med fors
Lavpriskatalysator hjælper med at omdanne havvand til brændstof i stor skalaKredit:Pixabay/CC0 Public Domain Søværnets søgen efter at drive sine skibe ved at omdanne havvand til brændstof er et skridt nærmere. University of Rochester kemiingeniører, i samarbejde med fors
- Pigmenter i oliemalerier forbundet med nedbrydning af kunstværker
- Hvordan kan du bevise, at der findes en magnetisk form af jern i jorden?
- En model til beskrivelse af menneskemængdenes hydrodynamik
- Vinregioner kan skrumpe dramatisk med klimaændringer, medmindre producenterne bytter sorter
- Instrumenter til måling af lufttryk
- Undersøgelsen sætter spørgsmålstegn ved gældende regler om lysforurening og opfordrer til et pa…


