Hvilken familie af elementer er den mest reaktive ikke -metale familie?
Her er hvorfor:
* Elektronaffinitet: Halogener har en meget høj elektronaffinitet, hvilket betyder, at de let får et elektron for at opnå en stabil octet -konfiguration. Dette gør dem meget reaktive med at vinde elektroner fra andre elementer.
* Elektronegativitet: Halogener er meget elektronegative, hvilket betyder, at de stærkt tiltrækker elektroner i en kemisk binding.
* reaktivitetstendenser: Når du bevæger dig ned ad halogengruppen (fra fluor til jod), falder reaktiviteten. Dette skyldes, at atomstørrelsen øges, hvilket gør det mindre let for atomet at tiltrække en elektron. Derfor er fluor den mest reaktive halogen.
Nøgle takeaways:
* Halogenerne (gruppe 17) er de mest reaktive ikke -metaller.
* Deres høje elektronaffinitet og elektronegativitet gør dem meget reaktive til at vinde elektroner.
* Fluor er den mest reaktive halogen.
Sidste artikelHvad er den maksimale mængde elektroner, som et atom kan donere, og hvorfor?
Næste artikelHvorfor flyder Puris på olie?
 Varme artikler
Varme artikler
-
 Strækbare superkondensatorer til at drive morgendagens bærbare enhederDisse skovlignende rækker af kulstofnanorør blev skabt på et elastomersubstrat, der blev forstrakt i én retning og derefter fik lov til at trække sig sammen. Denne proces skaber strækbare superkondens
Strækbare superkondensatorer til at drive morgendagens bærbare enhederDisse skovlignende rækker af kulstofnanorør blev skabt på et elastomersubstrat, der blev forstrakt i én retning og derefter fik lov til at trække sig sammen. Denne proces skaber strækbare superkondens -
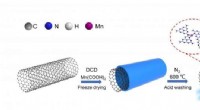 Mangan-enkeltatom-katalysator øger ydeevnen af elektrokemisk reduktion af kuldioxidSkematisk diagram af Mn SAC-fremstilling og mekanisme for elektrokemisk CO 2 reduktion. Kredit:FENG jiaqi Elektrokemisk CO 2 reduktionsreaktion (CO 2 RR) er en lovende tilgang til at omdanne
Mangan-enkeltatom-katalysator øger ydeevnen af elektrokemisk reduktion af kuldioxidSkematisk diagram af Mn SAC-fremstilling og mekanisme for elektrokemisk CO 2 reduktion. Kredit:FENG jiaqi Elektrokemisk CO 2 reduktionsreaktion (CO 2 RR) er en lovende tilgang til at omdanne -
 Afkodning af en nøgledel af cellen atom for atomKredit:Valerie Altounian Uanset hvad du laver, om det er at køre bil, gå en løbetur eller endda på din dovneste måde, spise chips og se tv på sofaen, er der en hel suite af molekylært maskineri ind
Afkodning af en nøgledel af cellen atom for atomKredit:Valerie Altounian Uanset hvad du laver, om det er at køre bil, gå en løbetur eller endda på din dovneste måde, spise chips og se tv på sofaen, er der en hel suite af molekylært maskineri ind -
 Forsker undersøger, hvordan man konverterer kuldioxid til byggestenene til brændstofBall-and-stick model af kuldioxid. Kredit:Wikipedia At opdele de kemiske bindinger i CO2 molekyler, er der brug for varme. En måde at få denne varme på er fra plasmaer, og det har længe været kendt
Forsker undersøger, hvordan man konverterer kuldioxid til byggestenene til brændstofBall-and-stick model af kuldioxid. Kredit:Wikipedia At opdele de kemiske bindinger i CO2 molekyler, er der brug for varme. En måde at få denne varme på er fra plasmaer, og det har længe været kendt
- Orkanen Delta svækkes, da den er på vej mod Mexico
- Hvor de reproduktive dele af en angiosperm placeret?
- En mulig ny måde at køle computerchips på
- Offentlige minoritetsledere foretrækker at integrere social lighed, traditionelle offentlige værdi…
- Sådan fortæller du kønsforskel i Sandhill Cranes
- Kryptovalutaer bliver endelig mainstream - kampen står i gang for at bringe dem under global kontro…


