Hvad er pH på 535 ml gasformig HCI ved 26,5 grader C og 747 mmHg opløst i nok vand til at fremstille 625 ml opløsning?
1. Beregn molen af HCL
* Konverter pres til atmosfærer: 747 mmHg * (1 atm / 760 mmHg) =0,983 atm
* Konverter temperatur til Kelvin: 26,5 ° C + 273,15 =299,65 K
* Brug den ideelle gaslov: PV =NRT
* n =(PV) / (RT)
* n =(0,983 atm * 0,535 l) / (0,0821 L * ATM / mol * K * 299,65 K) =0,0214 mol HCI
2. Beregn molariteten af HCL -løsningen
* molaritet (m) =mol opløst / liter opløsning
* M =0,0214 mol / 0,625 L =0,0342 m
3. Beregn pH
* HCL er en stærk syre, så den adskiller sig fuldstændigt i vandet. Dette betyder, at koncentrationen af H+ -ioner er lig med koncentrationen af HCI.
* ph =-log [H+]
* ph =-log (0,0342) = 1,47
Derfor er pH -værdien for HCL -opløsningen ca. 1,47.
 Varme artikler
Varme artikler
-
 Ny forskning giver en superstærk aluminiumslegeringPurdue postdoktorale forskningsassocieret Sichuang Xue, til venstre, og doktorand Qiang Li, forberede en prøve til forskning for at skabe superstærke aluminiumslegeringer. Kredit:Purdue University bil
Ny forskning giver en superstærk aluminiumslegeringPurdue postdoktorale forskningsassocieret Sichuang Xue, til venstre, og doktorand Qiang Li, forberede en prøve til forskning for at skabe superstærke aluminiumslegeringer. Kredit:Purdue University bil -
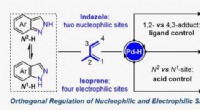 Ortogonal reguleringsstrategi giver nye muligheder for opbygning af molekylær kompleksitetPd-katalytisk regiodivergent dimethylallylering af indazol med isopren. Kredit:JIANG Wenshuang og JI Dingwei Dimethylallyl-relaterede enheder spiller en væsentlig rolle i at øge lipofilicitet af m
Ortogonal reguleringsstrategi giver nye muligheder for opbygning af molekylær kompleksitetPd-katalytisk regiodivergent dimethylallylering af indazol med isopren. Kredit:JIANG Wenshuang og JI Dingwei Dimethylallyl-relaterede enheder spiller en væsentlig rolle i at øge lipofilicitet af m -
 Holdbar belægning dræber COVID-virus og andre bakterier på få minutterBilledet forbliver klart selv gennem et tykt lag af den antimikrobielle belægning. Kredit:Anish Tuteja, University of Michigan Der kan snart være et nyt våben i vores århundreder gamle kamp mod bak
Holdbar belægning dræber COVID-virus og andre bakterier på få minutterBilledet forbliver klart selv gennem et tykt lag af den antimikrobielle belægning. Kredit:Anish Tuteja, University of Michigan Der kan snart være et nyt våben i vores århundreder gamle kamp mod bak -
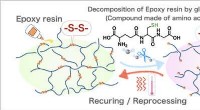 Ny strategi til fremme af genbrug af kulfiberforstærket plastFigur 1:Genbrugssystem af epoxyharpiks med peptidopløsning. Kredit:National Institute for Materials Science Epoxyharpiks er en type termohærdende harpiks, der almindeligvis anvendes i lim, maling
Ny strategi til fremme af genbrug af kulfiberforstærket plastFigur 1:Genbrugssystem af epoxyharpiks med peptidopløsning. Kredit:National Institute for Materials Science Epoxyharpiks er en type termohærdende harpiks, der almindeligvis anvendes i lim, maling
- Ligheder i solen og månen
- Forskere skal studere virkningen af COVID-19 og social distancering på familier
- Bioplast i bæredygtighedsdilemmaet
- Tanken om en miljøafgift er endelig ved at vinde styrke
- Anatomi af en kosmisk måge
- Hvordan arbejdsgivere kan forhindre erfarne ældre arbejdstagere i at gå på pension


