Har kulstof mere atomradius end germanium?
Her er hvorfor:
* atomstørrelsestrend: Atomradius øges generelt, når du bevæger dig ned ad en gruppe i den periodiske tabel. Dette skyldes, at antallet af elektronskaller øges, hvilket fører til et større atom.
* Position: Carbon og germanium er begge i gruppe 14 (også kendt som gruppe IV) af den periodiske tabel. Germanium er placeret under kulstof, hvilket betyder, at det har flere elektronskaller.
* afskærmningseffekt: De yderligere elektronskaller i germanium øger også afskærmningseffekten, hvor indre elektroner beskytter de ydre elektroner mod kernenes attraktive kraft. Dette bidrager yderligere til en større atomradius.
Derfor har germanium en større atomradius end kulstof.
 Varme artikler
Varme artikler
-
 For at lave aminosyrer, tilføj bare elektricitetEn demonstrationsflowreaktor konstrueret af forskere ved Kyushu University omdanner løbende kildematerialer til aminosyrer gennem en reaktion drevet af elektricitet. Ved at vælge den rigtige kombinati
For at lave aminosyrer, tilføj bare elektricitetEn demonstrationsflowreaktor konstrueret af forskere ved Kyushu University omdanner løbende kildematerialer til aminosyrer gennem en reaktion drevet af elektricitet. Ved at vælge den rigtige kombinati -
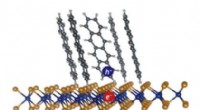 Hurtigt bevægende elektroner skaber strøm i organiske solcellerEn exciton (elektron-hul-par) dannet ved grænsefladen mellem tetracen-molekyler (en organisk halvleder) og enkeltlags WS2 (en uorganisk halvleder). Dissociation af sådanne grænseflade excitoner er nød
Hurtigt bevægende elektroner skaber strøm i organiske solcellerEn exciton (elektron-hul-par) dannet ved grænsefladen mellem tetracen-molekyler (en organisk halvleder) og enkeltlags WS2 (en uorganisk halvleder). Dissociation af sådanne grænseflade excitoner er nød -
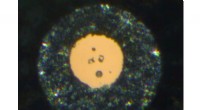 Højtryk skaber nye naboer til berylliumHurlbutitkrystaller (i midten) i diamantamboltcellen, der blev brugt til højtryksforsøgene. Krystallerne er hver omkring 0,01 millimeter store. Kredit:DESY, Anna Pakhomova Det sjældne grundstof be
Højtryk skaber nye naboer til berylliumHurlbutitkrystaller (i midten) i diamantamboltcellen, der blev brugt til højtryksforsøgene. Krystallerne er hver omkring 0,01 millimeter store. Kredit:DESY, Anna Pakhomova Det sjældne grundstof be -
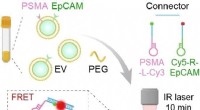 Hurtig, ukompliceret og specifik:Diagnose af prostatacancer fra blodprøverGrafisk abstrakt. Kredit:Angewandte Chemie International Edition (2022). DOI:10.1002/anie.202207037 Tidlig opdagelse af prostatacancer, en af de mest almindelige kræftformer hos mænd, opnås ofte
Hurtig, ukompliceret og specifik:Diagnose af prostatacancer fra blodprøverGrafisk abstrakt. Kredit:Angewandte Chemie International Edition (2022). DOI:10.1002/anie.202207037 Tidlig opdagelse af prostatacancer, en af de mest almindelige kræftformer hos mænd, opnås ofte
- Hvorfor er himlen høj ifølge Hiligaynon?
- Messeblues:Udstillinger bliver virtuelle, efterhånden som virus spredes
- Forebyggelse af giftige arbejdsmiljøer gennem etisk ledelse
- Beregn masse af klor, der kan dannes fra 50 g natriumchlorid?
- Det kinesiske kulforbud bærer et væsentligt politisk budskab
- Hvad bruges destillation til at adskille sig?


