Hvordan kan du ændre opløseligheden af et opløst stof?
1. Temperatur:
* faste stoffer og væsker: Generelt øger øget temperatur opløseligheden af faste stoffer og væsker i væsker. Dette skyldes, at højere temperaturer giver mere energi for, at de opløste partikler overvinder intermolekylære kræfter og opløses.
* Gasser: Stigende temperatur mindsker opløseligheden af gasser i væsker. Dette skyldes, at gasmolekyler har mere kinetisk energi ved højere temperaturer, hvilket gør dem mere tilbøjelige til at flygte fra opløsningen.
2. Tryk:
* Gasser: Stigende tryk øger opløseligheden af gasser i væsker. Dette skyldes Henrys lov, der siger, at opløseligheden af en gas er direkte proportional med det delvise tryk på gassen over væsken.
* faste stoffer og væsker: Tryk har en ubetydelig effekt på opløseligheden af faste stoffer og væsker.
3. Polaritet:
* "Ligesom opløser som" Princip: Opløsninger har en tendens til at opløses i opløsningsmidler med lignende polariteter.
* Polære opløste stoffer (f.eks. Sukker, salt) opløses godt i polære opløsningsmidler (f.eks. Vand).
* Ikke -polære opløste stoffer (f.eks. Olie, fedt) opløses godt i ikke -polære opløsningsmidler (f.eks. Hexan).
4. Partikelstørrelse:
* Mindre partikelstørrelse øger overfladearealet af opløsningen, hvilket fører til hurtigere opløsning. Dette skyldes, at der er flere kontaktpunkter mellem opløst og opløsningsmiddel.
5. Omrøring eller agitation:
* Omrøring eller agitation hjælper med at øge opløsningshastigheden ved at bringe frisk opløsningsmiddel i kontakt med opløsningen.
6. Tilføjelse af andre opløste stoffer:
* Tilstedeværelsen af andre opløste stoffer kan påvirke opløseligheden af et specifikt opløst stof. For eksempel kan tilsætning af en fælles ion til en opløsning reducere opløseligheden af et sparsomt opløseligt salt (almindelig ioneffekt).
7. Kemiske reaktioner:
* Nogle opløste stoffer reagerer med opløsningsmidlet for at danne nye forbindelser og ændre deres opløselighed. For eksempel danner opløsning af kuldioxid i vand kulsyre, som er mere opløselig end CO2 -gas.
8. Natur af opløst stof og opløsningsmiddel:
* De specifikke kemiske egenskaber ved opløst stof og opløsningsmiddel spiller en afgørende rolle i bestemmelsen af opløselighed. Faktorer såsom styrken af intermolekylære kræfter og størrelsen og formen af molekyler er vigtige.
Ved at manipulere disse faktorer kan man øge eller mindske opløseligheden af et opløst stof i et givet opløsningsmiddel.
 Varme artikler
Varme artikler
-
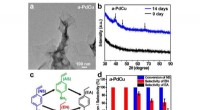 Heterofase nanostrukturer, der bidrager til effektiv katalyse(a) TEM-billede af a-PdCu nanoark. (b) XRD-mønstre af den som syntetiserede (0 dage) a-PdCu og a-PdCu efter ældning i 14 dage. (c) Hydrogeneringsreaktion af 4-nitrostyren (stuetemperatur, H2 ballon).
Heterofase nanostrukturer, der bidrager til effektiv katalyse(a) TEM-billede af a-PdCu nanoark. (b) XRD-mønstre af den som syntetiserede (0 dage) a-PdCu og a-PdCu efter ældning i 14 dage. (c) Hydrogeneringsreaktion af 4-nitrostyren (stuetemperatur, H2 ballon). -
 Røntgenbilleder viser, hvordan perioder med stress ændrede en istidshyæne til knoglenPalæontologen Jennifer Anné efterforsker en plettet hyæne. Forskerne brugte knogler fra disse moderne dyr som analoger for bedre at forstå 40, 000 år gamle hulehyænefossiler fra istiden. Kredit:Childr
Røntgenbilleder viser, hvordan perioder med stress ændrede en istidshyæne til knoglenPalæontologen Jennifer Anné efterforsker en plettet hyæne. Forskerne brugte knogler fra disse moderne dyr som analoger for bedre at forstå 40, 000 år gamle hulehyænefossiler fra istiden. Kredit:Childr -
 Nye forbindelser med anticarcinogene forbindelser syntetiseretInmaculada Fernández og Rocío Recio og Noureddine Khiar. Kredit:CSIC Stereokemi og asymmetrisk syntesegruppe ved Det Farmaceutiske Fakultet ved University of Sevilla, i samarbejde med Asymmetric S
Nye forbindelser med anticarcinogene forbindelser syntetiseretInmaculada Fernández og Rocío Recio og Noureddine Khiar. Kredit:CSIC Stereokemi og asymmetrisk syntesegruppe ved Det Farmaceutiske Fakultet ved University of Sevilla, i samarbejde med Asymmetric S -
 To bakterielle co-kulturer øger mikrobe co-nedbrydning af dicarboximid fungiciderGrafisk abstrakt. https://doi.org/10.1016/j.jhazmat.2020.123888 Dicarboximid fungicider dimethachlon, iprodion og procymidon er blevet meget brugt over hele verden til at kontrollere plantesygdomm
To bakterielle co-kulturer øger mikrobe co-nedbrydning af dicarboximid fungiciderGrafisk abstrakt. https://doi.org/10.1016/j.jhazmat.2020.123888 Dicarboximid fungicider dimethachlon, iprodion og procymidon er blevet meget brugt over hele verden til at kontrollere plantesygdomm
- Politiske aktørers manipulation af sociale medier er et problem i industriel skala, rapport finder
- Hvad hedder det tiende udkast til planet?
- At finde manglende netværksforbindelser kan hjælpe med at udvikle nye lægemidler, stoppe sygdom, …
- Hvad er fødevarekæden for en bladet havdrager?
- Sådan laver du en gummiboll ud af et æg
- Hvad er en soltebula, og hvordan forholder den sig til dannelsen af jorden?


