Observation under reaktionen af strontium og ilt?
Indledende opsætning:
* strontium: Et sølvhvid, blødt, reaktivt metal.
* ilt: En farveløs, lugtfri gas.
Reaktionsinitiering:
* Opvarmning: Strontium er meget reaktiv med ilt, så simpelthen at udsætte det for luft ved stuetemperatur vil resultere i en langsom oxidation. For at se en mere dramatisk reaktion skal du varme strontiumet. Dette kan gøres ved hjælp af en Bunsen -brænder eller anden varmekilde.
observationer under reaktionen:
* lys, intens flamme: Reaktionen er meget eksoterm og frigiver en betydelig mængde energi. Denne energi udsendes som en meget lys, rødlig-orange flamme.
* hvid pulverdannelse: Når strontium brænder, reagerer det med ilt for at danne strontiumoxid (SRO), et hvidt pulveragtigt fast stof. Dette pulver vil være synligt som en rest på overfladen af strontium eller i reaktionsbeholderen.
* varme og lys: Reaktionen producerer en betydelig mængde varme, som kan mærkes, hvis du er tæt på reaktionen.
Sikkerhedsforholdsregler:
* Meget eksoterm: Reaktionen er meget eksoterm og kan generere betydelig varme. Håndter reaktionen med forsigtighed og bær passende sikkerhedsudstyr, herunder sikkerhedsbriller og handsker.
* reaktivt metal: Strontium er et meget reaktivt metal. Undgå kontakt med hud og øjne.
* ilt: Oxygen er en stærk oxidation og kan understøtte forbrænding. Sørg for korrekt ventilation og undgå brandfarlige materialer.
Yderligere oplysninger:
* Reaktionen af strontium og ilt er et klassisk eksempel på en forbrændingsreaktion. Det involverer den hurtige reaktion mellem et stof og en oxidisator, der frigiver varme og lys.
* Reaktionen kan også producere en lille mængde strontiumperoxid (SRO2) sammen med strontiumoxid.
* Den lyse rød-orange flamme produceret af strontium bruges i fyrværkeri til at skabe en karakteristisk farve.
Vigtig note: Dette eksperiment bør kun udføres af en kvalificeret kemiker i laboratorieindstillinger på grund af de involverede farer.
Sidste artikelHvilken opløst stof hæver det kogende punkt med vand mest?
Næste artikelHvilken finder sted under en redoxreaktion?
 Varme artikler
Varme artikler
-
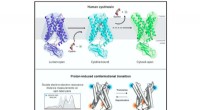 Undersøgelse afslører den molekylære oprindelse af den genetiske sygdom cystinoseStrukturelle og biofysiske undersøgelser af humant cystinosin afslører molekylære mekanismer og konformationel dynamik i protonkoblet lysosomal aminosyretransport. Kredit:Guo et al., Cell 2022 Den
Undersøgelse afslører den molekylære oprindelse af den genetiske sygdom cystinoseStrukturelle og biofysiske undersøgelser af humant cystinosin afslører molekylære mekanismer og konformationel dynamik i protonkoblet lysosomal aminosyretransport. Kredit:Guo et al., Cell 2022 Den -
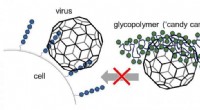 Kunstige slikstokke til at blokere viraDe kunstigt fremstillede glycomimetika (grønne) binder sig til viras bindingssteder, som vira normalt bruger til at binde til sukkerarter (blå) på celleoverfladen. Kredit:L. Hartmann, M. Schelhaas
Kunstige slikstokke til at blokere viraDe kunstigt fremstillede glycomimetika (grønne) binder sig til viras bindingssteder, som vira normalt bruger til at binde til sukkerarter (blå) på celleoverfladen. Kredit:L. Hartmann, M. Schelhaas -
 Opdagelse af en ny lov om faseadskillelseForskere ved University of Tokyo opdager en ny lov om, hvordan det komplekse netværk af faseadskilte strukturer vokser med tiden, hvilket kan føre til mere effektive batterier og industrielle katalysa
Opdagelse af en ny lov om faseadskillelseForskere ved University of Tokyo opdager en ny lov om, hvordan det komplekse netværk af faseadskilte strukturer vokser med tiden, hvilket kan føre til mere effektive batterier og industrielle katalysa -
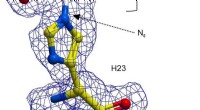 Kemikere viser, at det katalytiske udvalg af enzymer kan udvidesEn kugle-og-stik-repræsentation af H23 fra BH32 hæmmet med 2-bromacetophenon, farvet efter atomtype med H23 carbonatomer i gul og acetophenon carboner i hvid. Klar FEM elektrondensitet (blå, konturere
Kemikere viser, at det katalytiske udvalg af enzymer kan udvidesEn kugle-og-stik-repræsentation af H23 fra BH32 hæmmet med 2-bromacetophenon, farvet efter atomtype med H23 carbonatomer i gul og acetophenon carboner i hvid. Klar FEM elektrondensitet (blå, konturere
- Teknik kan gøre det lettere at bruge mRNA til at behandle sygdom eller levere vacciner
- Forskere udforsker maskinlæring for at automatisere sortering af mikrokapsler i realtid
- Undersøgelse detaljerede regulering af en multi-drug transporter
- Tidligste eksempel på en stor hydraulisk virksomhed udgravet i Kina
- Nærmeste eksoplanet endnu bekræftet af European Southern Observatory
- Akemikere låser op for hemmeligheder bag smeltede salte


