Hvilken gruppe på den periodiske tabel har den mest stabile mængde valenselektroner?
Her er hvorfor:
* Valenselektroner: Dette er elektronerne i den yderste skal af et atom, der er involveret i kemisk binding.
* stabilitet: Atomer er mest stabile, når deres yderste skal er fyldt med det maksimale antal elektroner, den kan indeholde.
* ædle gasser: Noble gasser har en fuld yderste skal, hvilket betyder, at de har en komplet oktet (8 valenselektroner) bortset fra helium, som har en komplet duet (2 valenselektroner). Dette gør dem meget ureaktive og stabile.
Eksempler:
* Helium (HE) - 2 Valenselektroner
* Neon (NE) - 8 Valenselektroner
* Argon (AR) - 8 Valenselektroner
* Krypton (KR) - 8 Valenselektroner
Fortæl mig, hvis du gerne vil udforske andre grupper og deres stabilitet!
 Varme artikler
Varme artikler
-
 En intelligent, formformende, selvhelbredende materiale til integreret kunstig muskel og nervevævForskere udvikler et formformende materiale med en hidtil uset multifunktionalitet til blød robotik og bærbar elektronik. Kredit:Soft Machines Lab, Carnegie Mellon University Fremskridt inden for
En intelligent, formformende, selvhelbredende materiale til integreret kunstig muskel og nervevævForskere udvikler et formformende materiale med en hidtil uset multifunktionalitet til blød robotik og bærbar elektronik. Kredit:Soft Machines Lab, Carnegie Mellon University Fremskridt inden for -
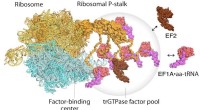 Højhastigheds atomkraftmikroskopi visualiserer celleproteinfabrikkerModel til oversættelse af ribosomer og forlængelsesfaktorer. EF1A • GTP • aatRNA og EF2 samles til den ribosomale stilk på det translaterende ribosom. Oversættelsesfaktorpuljen bidrager til effektiv p
Højhastigheds atomkraftmikroskopi visualiserer celleproteinfabrikkerModel til oversættelse af ribosomer og forlængelsesfaktorer. EF1A • GTP • aatRNA og EF2 samles til den ribosomale stilk på det translaterende ribosom. Oversættelsesfaktorpuljen bidrager til effektiv p -
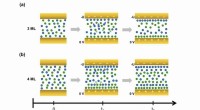 Forskere udvikler realtidsteknik til at studere ioniske væsker ved elektrodegrænsefladerTeamets forskning viste, at de ioniske rekonfigurationer, der forekommer nær guldelektroderne (gule stænger), afhænger af tykkelsen af de undersøgte ioniske flydende film, som illustreret i ovenståe
Forskere udvikler realtidsteknik til at studere ioniske væsker ved elektrodegrænsefladerTeamets forskning viste, at de ioniske rekonfigurationer, der forekommer nær guldelektroderne (gule stænger), afhænger af tykkelsen af de undersøgte ioniske flydende film, som illustreret i ovenståe -
 Kemiker skaber næste generation af neurovidenskabelige værktøjerRobert Campbell, professor i kemi, bygger nye værktøjer til neuroforskere i sit laboratorium på University of Alberta. Kredit:University of Alberta UAlberta kemiprofessor Robert Campbell udvikler
Kemiker skaber næste generation af neurovidenskabelige værktøjerRobert Campbell, professor i kemi, bygger nye værktøjer til neuroforskere i sit laboratorium på University of Alberta. Kredit:University of Alberta UAlberta kemiprofessor Robert Campbell udvikler
- Hvilke funktioner har urea?
- Hvor moderne var europæiske neandertalere?
- Hvad kunne naturligt udvælgelse ikke forekomme uden?
- NZ-Kina-aftalen har medført store økonomiske gevinster
- Undersøgelse viser i dag atmosfæriske kuldioxidniveauer på mere end 23 millioner års rekord
- Forskning i lipidnanopartikler nærmer sig genetiske behandlinger for arvelig lungesygdom, synstab


