Et molekyle med modsatte ladninger på enderne?
Her er hvorfor:
* Polaritet: Et molekyle er polært, når den ene ende har en lidt positiv ladning (δ+), og den anden ende har en lidt negativ ladning (Δ-). Denne forskel skyldes en ujævn fordeling af elektroner.
* Elektronegativitet: Den ujævne fordeling af elektroner opstår fra forskellen i elektronegativitet mellem atomerne i molekylet. Elektronegativitet er et atoms evne til at tiltrække elektroner mod sig selv i en binding.
* Atomer med højere elektronegativitet tiltrækker elektroner stærkere, hvilket skaber en delvis negativ ladning (Δ-) omkring dem.
* Atomer med lavere elektronegativitet har en delvis positiv ladning (Δ+).
Eksempler på polære molekyler:
* vand (H₂O): Oxygen er mere elektronegativ end brint, hvilket resulterer i en negativ ladning på iltatomet og en positiv ladning på hydrogenatomerne.
* hydrogenchlorid (HCL): Klor er mere elektronegativ end brint, hvilket skaber en negativ ladning på chloratomet og en positiv ladning på brintatomet.
* kuldioxid (co₂): Selvom hvert iltatom har en negativ ladning, er molekylet lineært og symmetrisk. Dette betyder, at ladningerne annullerer, hvilket gør molekylet overordnet ikke -polært.
Fortæl mig, hvis du gerne vil have flere detaljer om polære molekyler eller have andre spørgsmål!
Sidste artikelHvordan er den kemiske formel for en syre forskellig fra en base?
Næste artikelHvilken væske har det højeste vandpotentiale?
 Varme artikler
Varme artikler
-
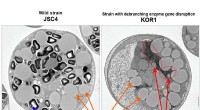 Ændring af kulhydrater til lipider til mikroalger biobrændstofferFigur 1:Elektronmikroskopbillede af lipidproduktion i mikroalgerne Chlamydomonas sp. Kredit:Kobe University Et tværinstitutionelt samarbejde har udviklet en teknik til at fordele kulstofressourcer
Ændring af kulhydrater til lipider til mikroalger biobrændstofferFigur 1:Elektronmikroskopbillede af lipidproduktion i mikroalgerne Chlamydomonas sp. Kredit:Kobe University Et tværinstitutionelt samarbejde har udviklet en teknik til at fordele kulstofressourcer -
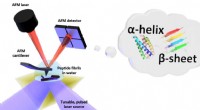 Formen i vand:Første nanoskalamålinger af biomolekylefoldning i væskeSkematisk af opsætningen for fototermisk induceret resonans (PTIR), som inkluderer en infrarød laserkilde og atomic force microscope (AFM) cantilever med en skarp spids, der rører prøven og vibrerer s
Formen i vand:Første nanoskalamålinger af biomolekylefoldning i væskeSkematisk af opsætningen for fototermisk induceret resonans (PTIR), som inkluderer en infrarød laserkilde og atomic force microscope (AFM) cantilever med en skarp spids, der rører prøven og vibrerer s -
 Hærforskere opdager magt i urinenMenneskelig urin er omkring 96 procent vand og fire procent affaldsstoffer, men der er mere end 3, 000 forbindelser findes i væsken. Hærforskere eksperimenterer med at producere brint fra urin. Kredit
Hærforskere opdager magt i urinenMenneskelig urin er omkring 96 procent vand og fire procent affaldsstoffer, men der er mere end 3, 000 forbindelser findes i væsken. Hærforskere eksperimenterer med at producere brint fra urin. Kredit -
 Forskere udvikler et effektivt system til levering af biomateriale til laboratorierKredit:National University of Science and Technology MISIS Materialeforskere fra NUST MISIS, sammen med kolleger fra Institut for Kemi ved Lomonosov Moscow State University, har udviklet en billig
Forskere udvikler et effektivt system til levering af biomateriale til laboratorierKredit:National University of Science and Technology MISIS Materialeforskere fra NUST MISIS, sammen med kolleger fra Institut for Kemi ved Lomonosov Moscow State University, har udviklet en billig
- Nyt brændstof for at få søfragten miljøvenlig skibsform
- Hvilken type bindinger danner saltsyre?
- Nepal taber til Kina, da Everest -operatører krydser bjerg
- Magnetisme driver metaller til isolatorer i nyt eksperiment
- Hvilken astronomerteori førte til store ændringer i videnskab og samfund?
- Mød AFM: Den forvirrende New Disease Nogle Læger Ring til den Nye Polio


