Er formlen for metan både en molekylær og en empirisk formel?
Her er hvorfor:
* molekylær formel: Denne formel repræsenterer det faktiske antal atomer for hvert element, der er til stede i et molekyle. Metan har et carbonatom og fire hydrogenatomer, så CH₄ afspejler nøjagtigt dens sammensætning.
* Empirisk formel: Denne formel viser det enkleste forhold mellem hele antal atomer i en forbindelse. I metan er forholdet mellem kulstof og brint 1:4, som allerede er det enkleste forhold mellem hele antal. Derfor er Ch₄ også den empiriske formel.
I tilfælde, hvor et molekyle har flere enheder med den samme empiriske formel, ville molekylformlen være anderledes. For eksempel er den empiriske formel for glukose Ch₂O, men dens molekylære formel er c₆h₁₂o₆. For metan falder imidlertid de molekylære og empiriske formler sammen.
 Varme artikler
Varme artikler
-
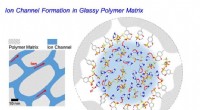 Vil stærk og hurtigt skiftende kunstig muskel være mulig?Skematisk diagram af ionkanaldannelse inde i polymerelektrolytten. Kredit:POSTECH I den amerikanske actionfilm Pacific Rim kæmper gigantiske robotter kaldet Jaegers mod ukendte monstre for at redde
Vil stærk og hurtigt skiftende kunstig muskel være mulig?Skematisk diagram af ionkanaldannelse inde i polymerelektrolytten. Kredit:POSTECH I den amerikanske actionfilm Pacific Rim kæmper gigantiske robotter kaldet Jaegers mod ukendte monstre for at redde -
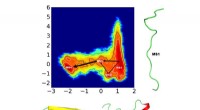 Ny metode fremskynder simuleringer, giver ny indsigt i proteinfoldningForskere søger at forstå proteinfoldning bedre for at helbrede fejlfoldningssygdomme, men denne utroligt komplekse proces kræver sofistikerede algoritmer til at identificere foldemekanismerne. Beregni
Ny metode fremskynder simuleringer, giver ny indsigt i proteinfoldningForskere søger at forstå proteinfoldning bedre for at helbrede fejlfoldningssygdomme, men denne utroligt komplekse proces kræver sofistikerede algoritmer til at identificere foldemekanismerne. Beregni -
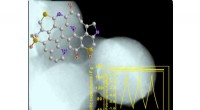 Højt nitrogen og svovl dobbelt-dopede kulstofmikrosfærer til superkondensatorerDenne figur viser morfologien, molekylær model og cyklisk ydeevne af den N/S co-doterede kulstofmikrosfære. Kredit:©Science China Press Blandt elektrodematerialer til superkondensatorer, kulstofba
Højt nitrogen og svovl dobbelt-dopede kulstofmikrosfærer til superkondensatorerDenne figur viser morfologien, molekylær model og cyklisk ydeevne af den N/S co-doterede kulstofmikrosfære. Kredit:©Science China Press Blandt elektrodematerialer til superkondensatorer, kulstofba -
 Ny metode til at forbinde præfabrikerede betonbjælker og søjlerAdjunkt Mostafa Tazarv fra Institut for Bygge- og Miljøteknik fører tilsyn med test af en ny metode til at forbinde præfabrikerede betonbjælker og søjler, der gør det muligt at reparere bygninger efte
Ny metode til at forbinde præfabrikerede betonbjælker og søjlerAdjunkt Mostafa Tazarv fra Institut for Bygge- og Miljøteknik fører tilsyn med test af en ny metode til at forbinde præfabrikerede betonbjælker og søjler, der gør det muligt at reparere bygninger efte


