Ved hvilken temperatur reagerer benzen med klor uden katalysator?
mekanisme:
1. initiering: UV -lys giver energien til at bryde klormolekylet (CL 2 ) i to klorradikaler (CL •).
2. Formering: Chlorradikalen angriber benzenringen og abstraherer et hydrogenatom og danner en benzenradikal. Denne radikal reagerer derefter med et andet klormolekyle til dannelse af chlorobenzen og en ny klorradikal og fortsætter kædereaktionen.
3. Opsigelse: Reaktionen afsluttes, når to radikaler kombineres for at danne et stabilt molekyle.
Bemærk: Denne reaktion er ikke meget selektiv og kan føre til dannelse af flere chlorerede produkter.
I fravær af en katalysator og UV -lys gør Benzenes høje elektrondensitet det relativt ureaktivt over for elektrofilt angreb fra klor.
 Varme artikler
Varme artikler
-
 Rumtemperaturkonvertering af CO2 til CO:En ny måde at syntetisere kulbrinter påIllustration af en ny stuetemperaturproces til fjernelse af kuldioxid (CO 2 ) ved at omdanne molekylet til kulilte (CO). I stedet for at bruge varme, nanoskalametoden er afhængig af energien fra ove
Rumtemperaturkonvertering af CO2 til CO:En ny måde at syntetisere kulbrinter påIllustration af en ny stuetemperaturproces til fjernelse af kuldioxid (CO 2 ) ved at omdanne molekylet til kulilte (CO). I stedet for at bruge varme, nanoskalametoden er afhængig af energien fra ove -
 Succes med at syntetisere sort fosfor med en sikker og højtydende metode til kunstig fotosynteseSyntetiseret sort fosfor. Kredit:Sakai Chemical Co., Ltd. / Osaka City University En fælles forskergruppe ved Osaka City University og Sakai Chemical Industry Co., Ltd. er lykkedes med at syntetis
Succes med at syntetisere sort fosfor med en sikker og højtydende metode til kunstig fotosynteseSyntetiseret sort fosfor. Kredit:Sakai Chemical Co., Ltd. / Osaka City University En fælles forskergruppe ved Osaka City University og Sakai Chemical Industry Co., Ltd. er lykkedes med at syntetis -
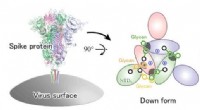 Glykaner er afgørende for COVID-19-infektionMolekylær mekanisme, der ligger til grund for den strukturelle ændring af SARS-CoV-2 spike-proteinet. Kredit:RIKEN En forskergruppe ved RIKEN Center for Computational Science (R-CCS) har fundet ud
Glykaner er afgørende for COVID-19-infektionMolekylær mekanisme, der ligger til grund for den strukturelle ændring af SARS-CoV-2 spike-proteinet. Kredit:RIKEN En forskergruppe ved RIKEN Center for Computational Science (R-CCS) har fundet ud -
 Retsmedicinsk kemiker foreslår svedteststrimmel som erstatning for alkometerUniversitetet i Albany retsmedicinsk kemiker Jan Halámek. Kredit:Paul Miller Retsmedicineren Jan Halámek har igen fundet en innovativ anvendelse til menneskelig sved - denne gang for at holde fuld
Retsmedicinsk kemiker foreslår svedteststrimmel som erstatning for alkometerUniversitetet i Albany retsmedicinsk kemiker Jan Halámek. Kredit:Paul Miller Retsmedicineren Jan Halámek har igen fundet en innovativ anvendelse til menneskelig sved - denne gang for at holde fuld
- Metaverset er her ikke endnu, men det har allerede en lang historie
- Hvordan beregner jeg gentagelighed?
- Ny katalysator muliggør energivenlig ammoniakproduktion til gødning og alternativt brændstof
- Første ting først:For at opfylde klimamålene, vi kan ikke springe lavere trin af afbødningshiera…
- Hvilket udtryk bruges til at beskrive reproducerbarheden af en måling?
- Hvorfor Alberta ville være tåbeligt at opgive kulstofpolitikken


