En reaktion, hvor produkter kan reagere på re-form reaktanter er?
Her er en mere detaljeret forklaring:
* reversible reaktioner er kemiske reaktioner, der kan fortsætte i både fremadgående og omvendte retninger. Dette betyder, at reaktionens produkter kan reagere med hinanden for at danne de originale reaktanter.
* ligevægt er en tilstand, hvor hastighederne for de fremadgående og omvendte reaktioner er ens. Ved ligevægt forbliver koncentrationerne af reaktanter og produkter konstante, selvom reaktionen stadig forekommer.
* dobbeltpile bruges i kemiske ligninger til at repræsentere reversible reaktioner. For eksempel:
`` `
A + B ⇌ C + D
`` `
Denne ligning indikerer, at A og B kan reagere på form C og D, og vice versa.
Eksempler på reversible reaktioner:
* syntesen af ammoniak:
`` `
N₂ (g) + 3H₂ (g) ⇌ 2nh₃ (g)
`` `
* Ionisering af vand:
`` `
H₂O (L) ⇌ H⁺ (aq) + OH⁻ (aq)
`` `
* Reaktionen af kuldioxid med vand:
`` `
Co₂ (g) + h₂o (l) ⇌ h₂co₃ (aq)
`` `
Fortæl mig, hvis du gerne vil vide mere om reversible reaktioner eller ligevægt!
Sidste artikelHvorfor natrium og magnesium valens 1?
Næste artikelHvad er det sværeste stof på jorden, der ikke er metal?
 Varme artikler
Varme artikler
-
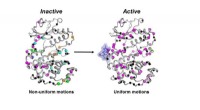 Enzymbevægelse kan være nøglen til nye kræftlægemidlerDen inaktive form (venstre) af MAPK p38-enzymet bevæger sig på en ukoordineret måde. Når de nødvendige molekyler (blå klat og P-symboler) binder, enzymet bliver aktivt (til højre) ved at bevæge sig på
Enzymbevægelse kan være nøglen til nye kræftlægemidlerDen inaktive form (venstre) af MAPK p38-enzymet bevæger sig på en ukoordineret måde. Når de nødvendige molekyler (blå klat og P-symboler) binder, enzymet bliver aktivt (til højre) ved at bevæge sig på -
 En hydrogel, der klæber godt til brusk og meniskKredit:Ecole Polytechnique Federale de Lausanne EPFL-forskere har udviklet en hydrogel – bestående af næsten 90 % vand – som naturligt klæber til blødt væv som brusk og menisken. Hvis hydrogelen b
En hydrogel, der klæber godt til brusk og meniskKredit:Ecole Polytechnique Federale de Lausanne EPFL-forskere har udviklet en hydrogel – bestående af næsten 90 % vand – som naturligt klæber til blødt væv som brusk og menisken. Hvis hydrogelen b -
 Forskere fremstiller alsidig katalysator til polyestersyntese og nedbrydningZn(HMDS)2 som en alsidig transesterificeringskatalysator til polyestersyntese og nedbrydning. Kredit:XU Guangqiang Hvid forurening fra kasseret plastaffald er et af de mest presserende miljøproble
Forskere fremstiller alsidig katalysator til polyestersyntese og nedbrydningZn(HMDS)2 som en alsidig transesterificeringskatalysator til polyestersyntese og nedbrydning. Kredit:XU Guangqiang Hvid forurening fra kasseret plastaffald er et af de mest presserende miljøproble -
 Nyt batteridesign kan oplade en elbil på 10 minutterEt hurtigopladningsbatteri opfundet af Chao-Yang Wang Group. Kredit:Chao-Yang Wang Group Ti minutters opladningstid for at tilføje 200 miles af køreafstand:Forskere i USA har hævdet et teknologisk
Nyt batteridesign kan oplade en elbil på 10 minutterEt hurtigopladningsbatteri opfundet af Chao-Yang Wang Group. Kredit:Chao-Yang Wang Group Ti minutters opladningstid for at tilføje 200 miles af køreafstand:Forskere i USA har hævdet et teknologisk
- Brug af maskinlæring til at opdage upålidelige Facebook -sider
- Analyse af virkningen af college-gameday-hjem i det amerikanske syd
- Hvilket udtryk beskriver bakterier, der er runde eller sfærisk formede?
- En undersøgelse af nazistisk besættelse af bevægelse afslører yderligere, hvordan de fremstilled…
- Billede:Hubbles nærbillede af spiralskive, bule
- Efterligner enzymer, kemikere producerer store, nyttige carbonringe


