Hvad er oxidationstilstanden for hvert element i SO3 -2?
regler, der skal huskes:
* Oxygen's oxidationstilstand er typisk -2 undtagen i peroxider (hvor det er -1) og når det er bundet til fluor (hvor det er positivt).
* Summen af oxidationstilstandene i en polyatomisk ion skal svare til ladningen af ionen.
Anvendelse af reglerne:
1. ilt: Vi har tre iltatomer, hver med en oxidationstilstand på -2. Dette bidrager i alt 3 * (-2) =-6 til den samlede opladning.
2. svovl: Da sulfitionen (SO₃⁻²) har en ladning på -2, og iltatomerne bidrager -6, skal svovlatomet have en oxidationstilstand på +4 for at afbalancere det.
Derfor er oxidationstilstandene:
* svovl (r):+4
* ilt (O):-2
Sidste artikelHvad er oxidationstilstanden i hvert element i COH2?
Næste artikelHvad er oxidationstilstanden for et element?
 Varme artikler
Varme artikler
-
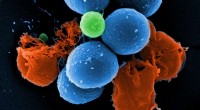 Modificeret kræftlægemiddel effektivt mod multiresistente bakterierScanningselektronmikrografi af intakt MRSA (blå), PK150-induceret vesikeldannelse (grøn), og MRSA ødelagt af PK150 (rød). Kredit:Manfred Rohde / HZI Antibiotika-resistente bakterier er i stigende
Modificeret kræftlægemiddel effektivt mod multiresistente bakterierScanningselektronmikrografi af intakt MRSA (blå), PK150-induceret vesikeldannelse (grøn), og MRSA ødelagt af PK150 (rød). Kredit:Manfred Rohde / HZI Antibiotika-resistente bakterier er i stigende -
 Forskere opdager ny strategi for udvikling af menneskeintegreret elektronikKredit:Unsplash/CC0 Public Domain Polymerhalvledere - materialer, der er blevet gjort bløde og elastiske, men stadig i stand til at lede elektricitet - lover fremtidig elektronik, der kan integrer
Forskere opdager ny strategi for udvikling af menneskeintegreret elektronikKredit:Unsplash/CC0 Public Domain Polymerhalvledere - materialer, der er blevet gjort bløde og elastiske, men stadig i stand til at lede elektricitet - lover fremtidig elektronik, der kan integrer -
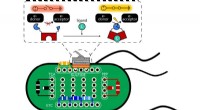 Switch-in-a-celle elektrificerer livetRice University forskere brugte E coli bakterier som en platform til at teste proteinkontakter, der kan bruges til at kontrollere strømmen af elektroner. Proteiner placeret i celler kan simpelthen
Switch-in-a-celle elektrificerer livetRice University forskere brugte E coli bakterier som en platform til at teste proteinkontakter, der kan bruges til at kontrollere strømmen af elektroner. Proteiner placeret i celler kan simpelthen -
 Hyperpolariseret proton -MR bruges til at observere metaboliske processer i realtidFantomet brugt til hyperpolariseret billeddannelse, med en illustration af billedskiver erhvervet ved hjælp af den nye teknik. Kredit:©:Laurynas Dagys, University of Southampton Magnetic resonance
Hyperpolariseret proton -MR bruges til at observere metaboliske processer i realtidFantomet brugt til hyperpolariseret billeddannelse, med en illustration af billedskiver erhvervet ved hjælp af den nye teknik. Kredit:©:Laurynas Dagys, University of Southampton Magnetic resonance
- Kan vi reducere partisk fjendskab? Ny analyse finder lovende i tidligere forskning
- Et øjebliksbillede af vores mystiske forfader Homo erectus
- Et problem med den kvantitative undersøgelse af magnesiumoxid er, at også reagerer, hvilke andre k…
- Simuleringer giver en potentiel forklaring på mystisk kløft i størrelsesfordelingen af superjor…
- Hvad er fælles for tværbølger og langsgående bølger?
- Nostalgi er ikke, hvad den plejede at være


