Shigella-bakterien udnytter en fysisk kraft kaldet endocytose i cellernes membran
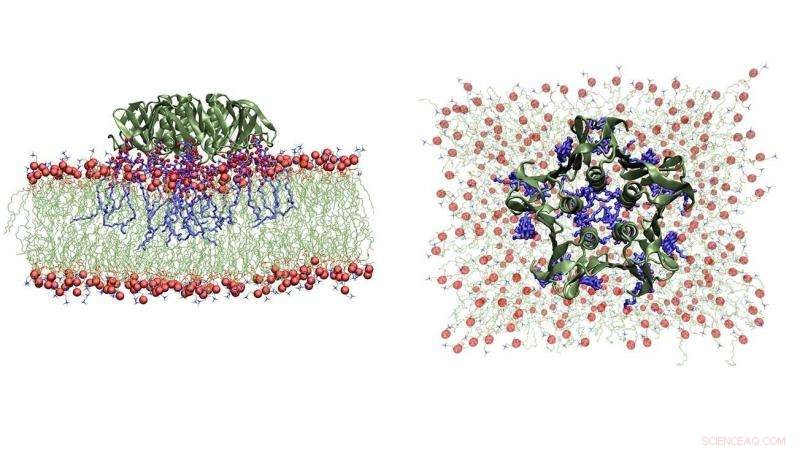
Snapshots fra en Molecular Dynamics-simulering af en enkelt shigella-toksinpartikel, der binder til dens lipidpartnere i vesikelmembranen (side- og topvisninger). Kredit:Julian Shillcock/EPFL
Bakterierne, der forårsager shigella-tarmsygdommen, bruger et toksin, der udnytter en fysisk kraft i cellernes membran. Selvom det er svært at blokere, det er muligt at kæmpe med nanopartikler, der udnytter den samme kraft.
Et enormt antal sygdomme er et resultat af bakterie- og virusinfektioner. Disse patogener kommer ind i kroppens celler gennem flere ruter. En ny undersøgelse i fællesskab ledet af EPFL rapporterer nu opdagelsen af en hidtil ukendt infektionsrute brugt af bakterierne, der forårsager shigellose, en tarminfektionssygdom karakteriseret ved blodig diarré. I den nyopdagede mekanisme, Shigella-bakterien udnytter en generisk kraft, der skabes af fluktuationerne i cellens egen plasmamembran. Værket er udgivet i ACS Nano .
Undersøgelsen er udført af John Ipsen ved Syddansk Universitet, Ludger Johannes ved Institut Curie i Frankrig og Julian Shillcock ved EPFL.
Normalt, celler regulerer indtrængen af fremmed materiale meget tæt, at forhindre invasioner fra patogener som bakterier og vira. Som resultat, angriberne har udviklet forskellige mekanismer til at overvinde barriererne og få adgang til celler.
For eksempel, en rute går ud på at kapre cellens eget maskineri og narre den til at internalisere virussen eller bakterien inde i en vesikel, som cellen selv laver. denne proces, som er en af de regelmæssige måder, celler optager store molekyler på, kaldes "endocytose".
Forskerne brugte forskellige vesikelsystemer og computersimuleringer til at studere en bakteriel invasionsmekanisme, der ser ud til at have nogle unikke egenskaber. Mekanismen bruges, blandt andre, af de bakterier, der forårsager shigella, og som producerer en lille, stift protein kaldet Shiga-toksin.
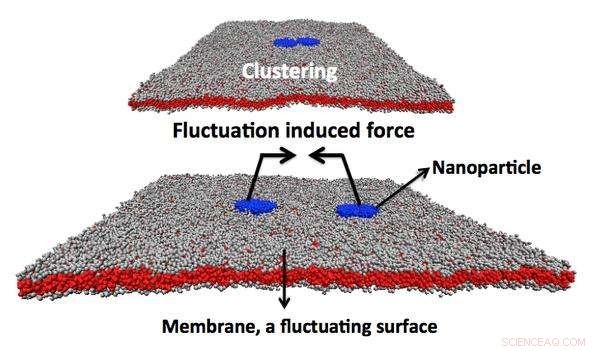
Illustration af en dissipativ partikeldynamiksimulering, der viser to tæt bundne toksiner bundet sammen af den Casimir-lignende kraft. Kredit:Julian Shillcock/EPFL
Undersøgelsen viste, at Shiga -toksinpartikler binder tæt til visse lipider, eller fedtstoffer, på membranoverfladen af den celle, der skal invaderes. De begynder derefter at danne klynger på membranen, som får membranen til at bue indad, skabe rørformede invaginationer, hvorigennem toksinpartiklerne kommer ind i cellen. En gang indenfor, Shiga-toksinerne ændrer cellens genetiske mekanisme, og infektionen er begyndt.
Men den største opdagelse var, at toksinet faktisk udnytter en generisk, fysisk kraft i cellens membran til at producere invaginationerne. Dette kaldes "Casimir -kraften" og blev først beskrevet som en teoretisk kraft, der virker mellem to ladede, parallel, ledende overflader.
Med hensyn til biologi, Casimir-kraften menes at virke mellem membranbundne proteiner i celler, eksisterer på alle flydende biologiske cellemembraner og opstår kun, når patogenet binder tæt til membranoverfladen.
Forskerne foreslår, at Shigella-bakterier, og andre patogener, har udviklet sig til at drage fordel af Casimir -kraften, der stammer fra den svingende plasmamembran til at inficere celler. Ud over, fordi de fedtstoffer, som toksinet binder til, bruges af cellen til dens egne operationer, Shiga-toksinet kan ikke blokeres fra at komme ind uden at deaktivere eller ændre cellens normale funktioner.
Nanopartikler til levering af lægemidler
Men fordi Casimir-kraften menes at opstå for eventuelle tæt bundne nanopartikler på overfladen af cellens membran, der er potentiale for at producere en roman, nanopartikelbaseret vej til lægemiddellevering. Først, vi bliver nødt til at binde nanopartikler tæt til overfladen af cellen, hvor de vil klynge sig sammen. Sekund, nanopartiklerne skal også øge cellemembranens krumning lidt for at udnytte Casimir-kraften og få adgang til cellen. En gang indenfor, de kan begynde at gøre gavn, defensive ændringer i cellens adfærd.
"Hvor naturen har ført til at udvikle et middel til patogener til at inficere celler, fremstillede nanopartikler kan følge for at behandle cellulær dysfunktion, " siger Julian Shillcock.
Sidste artikelForskere opdager en ny stoftilstand for vand
Næste artikelNanoskala samtaler skaber komplekse, flerlagsstrukturer
 Varme artikler
Varme artikler
-
 Nanospears leverer genetisk materiale til celler med stor nøjagtighedKredit:American Chemical Society UCLA-forskere har udviklet en ny metode, der anvender mikroskopiske splinterlignende strukturer kaldet nanospears til målrettet levering af biomolekyler såsom gene
Nanospears leverer genetisk materiale til celler med stor nøjagtighedKredit:American Chemical Society UCLA-forskere har udviklet en ny metode, der anvender mikroskopiske splinterlignende strukturer kaldet nanospears til målrettet levering af biomolekyler såsom gene -
 Flagelignende nanopartikler giver pålidelig rustbeskyttelseNanopartikler af zink-phosphat af flagetypen øger gasbarrieren for korrosionsbeskyttelse i stål. Kredit:INM/Uwe Bellhäuser Store mængder stål bruges i arkitektur, brobygning og skibsbygning. Struk
Flagelignende nanopartikler giver pålidelig rustbeskyttelseNanopartikler af zink-phosphat af flagetypen øger gasbarrieren for korrosionsbeskyttelse i stål. Kredit:INM/Uwe Bellhäuser Store mængder stål bruges i arkitektur, brobygning og skibsbygning. Struk -
 Låsning af mælkeformel kunne redde liv, siger videnskabsmænd(Phys.org) — En ny undersøgelse af fordøjelsen af mælk kan føre til udviklingen af nye formler til for tidligt fødte børn, vægttabsdrikke og potentielt nye lægemiddelleveringssystemer. Udgivet i
Låsning af mælkeformel kunne redde liv, siger videnskabsmænd(Phys.org) — En ny undersøgelse af fordøjelsen af mælk kan føre til udviklingen af nye formler til for tidligt fødte børn, vægttabsdrikke og potentielt nye lægemiddelleveringssystemer. Udgivet i -
 Risikoprofilering af nanomaterialer sætter sikkerhed førstKredit:Shutterstock Med usikkerhed omkring risikoen for, at nanomaterialer hæmmer EUs innovative potentiale, forskere arbejder på et sikkerhedskoncept for bedre at overvåge denne nye teknologi. F
Risikoprofilering af nanomaterialer sætter sikkerhed førstKredit:Shutterstock Med usikkerhed omkring risikoen for, at nanomaterialer hæmmer EUs innovative potentiale, forskere arbejder på et sikkerhedskoncept for bedre at overvåge denne nye teknologi. F
- Selvstændig samling i flere trin åbner døren til nye rekonfigurerbare materialer
- Informationstyveri via manipulering af skærmens lysstyrke i computere med luftspalte
- Kosmiske magnetfelter med forbløffende orden
- Nyt online værktøj hjælper bedre med at tjene miljømæssig retfærdighed
- Nr. 2 hvis til søs:Udhus bundet til Paul Revere udgraves
- Udbredte fejlklassificeringer får obligationsfonde til at fremstå langt mindre risikable, påvirke…


