Opdagelse af bruskheling i dyremodeller kan føre til nye menneskelige terapier
Forskere håber, at deres opdagelse om de helbredende egenskaber af føtale bruskceller i mus vil lægge grunden til nye behandlinger for menneskelige vækstforstyrrelser og degenerative sygdomme.
Udgivet i Nature Communications , fandt det Monash University-ledede projekt ud af, at når nogle føtale mus bruskceller døde, kunne bruskregionen heles inden for en uge. Det identificerede også et cellekommunikationssystem, der lettede helingen og kunne være et potentielt terapimål.
Førsteforfatter Dr. Chee Ho H'ng, en post-doc stipendiat ved Monash University's Australian Regenerative Medicine Institute, forklarede, at brusken, der normalt giver næring til knoglevækst og beklædning af menneskelige led, er blandt de væv med de værste reparationsevner af ethvert voksent menneske. væv.
Han sagde, at forskere ved at bruge mus observerede bruskområder, der kom sig, efter at nogle celler døde.
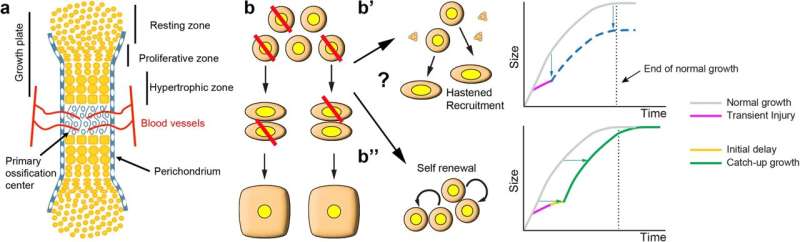
"Vi opdagede, at brusken heler inden for en uge, hvilket tillader knoglevækst at genoptage normalt," sagde Dr. H'ng. "Dette opnås ved først at genopbygge en pulje af celler med potentiale til at regenerere resten af brusken, og derefter accelerere deres progression i retning af at danne mere brusk.
"Vi fandt yderligere et celle-celle-kommunikationssystem, der er påkrævet for denne adfærdsændring, hvilket afslører et potentielt mål for fremtidige terapier."
Seniorforfatter Dr. Alberto Roseello-Diez sammenlignede opdagelsen med at håndtere en utæt brændstoftank. "Forestil dig, at du konkurrerer i et rallybilløb, og din brændstoftank bliver gennemboret og mister en del af brændstoffet," sagde han.
"Hvis du bare lapper det sammen og fortsætter med at køre, vil du løbe tør for brændstof, før du når slutningen. Men hvis du bruger lidt tid på at tanke op fra en reservetank, vil du, når du genoptager kapsejladsen, være i stand til at køre længere og indhente det. ."
Det er første gang, at en genetisk model er blevet brugt til at udløse forbigående ensidig celledød i lemmerbrusken, hvilket afslører potentielle reparationsmekanismer.
"Det giver en cellulær og molekylær forklaring på et klassisk fænomen kendt som catch-up vækst:genopretningen af en normal vækstbane efter en midlertidig vækstforsinkelse," sagde Dr. Rosello-Diez.
Dr. Rosello-Diez sagde, at der var behov for mere forskning med brug af menneskelige bruskorganoider og i sidste ende menneskelige forsøg, men resultaterne kunne give en model for terapier, der kan hjælpe med at stimulere bruskreparation i menneskelige vækstpladeskader.
Han sagde, at disse sandsynligvis var 10-15 år tilbage, da de skulle kombineres med cellulære terapier for at målrette mod vækstforstyrrelser.
"Terapier til bruskreparation kan i sidste ende føre til behandlinger for vækstforstyrrelser såsom dværgvækst og degenerative sygdomme såsom slidgigt," sagde han.
Flere oplysninger: Chee Ho H'ng et al., Kompensatorisk vækst og genopretning af bruskcytoarkitektur efter forbigående celledød i føtale muselemmer, Nature Communications (2024). DOI:10.1038/s41467-024-47311-7
Journaloplysninger: Nature Communications
Leveret af Monash University
 Varme artikler
Varme artikler
-
 Hvordan udvikler genomer sig mellem arter? Team udforsker 3D-strukturens nøglerolle i mandlige køn…Kredit:CC0 Public Domain En undersøgelse ledet af forskere ved Universitat Autònoma de Barcelona (UAB) og University of Kent afslører, hvordan genomets tredimensionelle struktur af mandlige kønscel
Hvordan udvikler genomer sig mellem arter? Team udforsker 3D-strukturens nøglerolle i mandlige køn…Kredit:CC0 Public Domain En undersøgelse ledet af forskere ved Universitat Autònoma de Barcelona (UAB) og University of Kent afslører, hvordan genomets tredimensionelle struktur af mandlige kønscel -
 Hvad gør jord, jord? Forskere finder skjulte spor i DNABotswana jordskorpe fundet på tur til landet. Kredit:Dr. Kelly Ramirez - Netherlands Institute of Ecology (NIOO-KNAW) Har du nogensinde spekuleret på, hvad der gør en jord, jord? Og kunne jord fra
Hvad gør jord, jord? Forskere finder skjulte spor i DNABotswana jordskorpe fundet på tur til landet. Kredit:Dr. Kelly Ramirez - Netherlands Institute of Ecology (NIOO-KNAW) Har du nogensinde spekuleret på, hvad der gør en jord, jord? Og kunne jord fra -
 DNA -forskere opfordrer knogleholdere til at dele knogleadgangMenneskelige rester fra arkæologiske udgravninger kan indeholde værdifuldt genetisk materiale. Forfatterne til et brev i tidsskriftet Nature har opfordret til mere åbenhed og adgang til forskning. Ari
DNA -forskere opfordrer knogleholdere til at dele knogleadgangMenneskelige rester fra arkæologiske udgravninger kan indeholde værdifuldt genetisk materiale. Forfatterne til et brev i tidsskriftet Nature har opfordret til mere åbenhed og adgang til forskning. Ari -
 Brug øjne på himlen til at lokalisere sæler i et hurtigt skiftende ArktisRingsælen ved siden af sit åndehul på fastisen ved St. Jonsfjorden, Svalbard. Kredit:Aeria (Eelke Folmer)/NIOZ/WUR I sommer lykkedes det forskerne at indsamle fantastiske dronebilleder af både ri
Brug øjne på himlen til at lokalisere sæler i et hurtigt skiftende ArktisRingsælen ved siden af sit åndehul på fastisen ved St. Jonsfjorden, Svalbard. Kredit:Aeria (Eelke Folmer)/NIOZ/WUR I sommer lykkedes det forskerne at indsamle fantastiske dronebilleder af både ri
- Dinosaurer med fjer var endnu mere luftige, end vi troede
- Undersøgelsen bruger ringe i tænderne til at forstå det miljø, neandertalerne stod over for
- Overgangen til en kulstoffattig økonomi skal være inklusiv, siger forskere
- Gammelt skibsvrag skal gøres tilgængeligt for dykkere i Grækenland
- Cthulhu fossile rekonstruktion afslører monstrøse slægtninge til moderne havagurker
- Sunkne lystbåde afslører den skjulte historie i Californien og videre


