Forskere afslører PI3K-enzymer med dobbelt accelerator- og bremsemekanismer
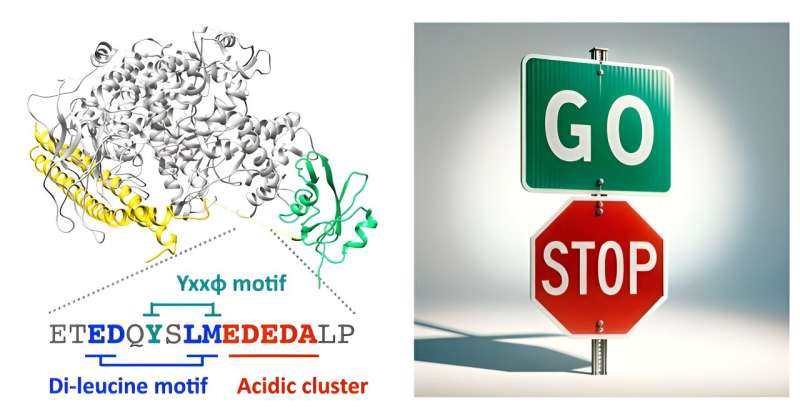
En gruppe forskere har udvidet konventionel viden om et kritisk enzym, der styrer cellemigration. I en publikation i tidsskriftet Nature Communications , rapporterede de, at phosphoinositide 3-kinase (PI3K) ikke kun virker som en accelerator til at fremskynde cellemotilitet, men den har også en indbygget bremsemekanisme, der hindrer migration.
"PI3K er et vigtigt signalenzym, der er blevet grundigt undersøgt i over 30 år på grund af dets roller i fundamentale cellulære funktioner som vækst, overlevelse, bevægelse og metabolisme," siger Hideaki Matsubayashi, hovedforfatter af undersøgelsen og assisterende professor ved Tohoku University's Frontier Forskningsinstituttet for Tværfaglige Videnskaber (FRIS).
"Det spiller en kritisk rolle i cellemigration og -invasion, noget der, når det er dysreguleret, kan forårsage mange patologier. Vores arbejde afslørede, at PI3K også aktivt kan begrænse de samme migrationsprocesser gennem en separat ikke-katalytisk endocytisk mekanisme, der stammer fra dens p85β-underenhed. "
Ved hjælp af en kombination af bioinformatik, molekylær modellering, biokemiske bindingsassays og levende-celle-billeddannelse, viser Matsubayashi og hans kolleger, at en forstyrret region inden for p85β's inter-SH2-domæne binder direkte til det endocytiske protein AP2. Denne del af PI3K kan aktivere en cellulær proces, der trækker visse molekyler ind i cellen, og den gør det uden behov for enzymets typiske lipidmodifikationsfunktion.
Da forskerne afbrød bindingen, fungerede den muterede p85β ikke, som den skulle. I stedet for at regulere cellens bevægelse gennem sin bremsemekanisme, byggede den sig op på specifikke steder i cellen. Dette fører til, at celler bevæger sig hurtigere og mere vedvarende, hvilket indikerer et tab af bremsemekanismens kontrol over cellemigration.
"Det er bemærkelsesværdigt, at dette enkelte PI3K-enzym har modsatrettede speeder- og bremsepedaler indbygget i dets molekylære ramme," tilføjer Matsubayashi. "Den endocytiske mekanisme hjælper med at regulere PI3K's aktivitet for at sikre, at cellebevægelsen kontrolleres på de rigtige tidspunkter og på de rigtige steder for vigtige biologiske processer."
Denne bremserolle viste sig at være specifik for kun p85β-underenheden. Og da p85β-underenheden af PI3K er forbundet med kræftfremmende egenskaber, kan en dybere forståelse af PI3K-regulering og dens isoformspecificitet føre til nye terapeutiske strategier, såsom dem, der selektivt hæmmer det cancerøse aspekt af PI3K, mens de normale funktioner af PI3K bevares. i raske celler.
Flere oplysninger: Hideaki T. Matsubayashi et al., Ikke-katalytisk rolle af phosphoinositide 3-kinase i mesenkymal cellemigration gennem ikke-kanonisk induktion af p85β/AP2-medieret endocytose, Nature Communications (2024). DOI:10.1038/s41467-024-46855-y
Journaloplysninger: Nature Communications
Leveret af Tohoku University
 Varme artikler
Varme artikler
-
 Matematik gør det muligt for videnskabsmænd at forstå organisationen i en cellekerneKlasser af transkriptionsklynger. I en selvbærende transkriptionsklynge er en TF og genet, der koder for den TF, begge til stede. De inter- og intrakromosomale eksempler i henholdsvis (a) og (b) illus
Matematik gør det muligt for videnskabsmænd at forstå organisationen i en cellekerneKlasser af transkriptionsklynger. I en selvbærende transkriptionsklynge er en TF og genet, der koder for den TF, begge til stede. De inter- og intrakromosomale eksempler i henholdsvis (a) og (b) illus -
 Er vi født med et moralsk kompas?Kredit:Unsplash/CC0 Public Domain I årtusinder har filosoffer overvejet spørgsmålet om, hvorvidt mennesker i sagens natur er gode. Men nu har forskere fra Japan fundet ud af, at unge spædbørn kan t
Er vi født med et moralsk kompas?Kredit:Unsplash/CC0 Public Domain I årtusinder har filosoffer overvejet spørgsmålet om, hvorvidt mennesker i sagens natur er gode. Men nu har forskere fra Japan fundet ud af, at unge spædbørn kan t -
 Kvindelig makak på italiensk helligdom spiste sin mumificerede døde babyTonkeansk sort makak. Kredit:Public Domain (Phys.org) – En trio af forskere, der arbejder på det italienske dyrereservat Parco Abatino, rapporterer, at de er vidne til en voksen hun Tonkean-makak
Kvindelig makak på italiensk helligdom spiste sin mumificerede døde babyTonkeansk sort makak. Kredit:Public Domain (Phys.org) – En trio af forskere, der arbejder på det italienske dyrereservat Parco Abatino, rapporterer, at de er vidne til en voksen hun Tonkean-makak -
 Bliver vi virkelig klogere med alderen?Uglen, den kloge gamle forsker i dyreverdenen. Se flere sunde aldringsbilleder. Yamada Taro/Riser/Getty Images I mange kulturer, uglen repræsenterer visdom. Fra en forening med Athena, den græske vis
Bliver vi virkelig klogere med alderen?Uglen, den kloge gamle forsker i dyreverdenen. Se flere sunde aldringsbilleder. Yamada Taro/Riser/Getty Images I mange kulturer, uglen repræsenterer visdom. Fra en forening med Athena, den græske vis
- Harlan Ellison, science fiction mester, dør i en alder af 84
- Ny undersøgelse om udfasning af kul giver anledning til tvivl om commissionitis
- Illegale jægere er et større problem på gårde end dyreaktivister
- Fem millioner års klimaforandringer bevaret ét sted
- Hvordan påvirker højden vejret?
- Udnyttelse af naturlige landskabers kraft til at udrydde skadedyr


