Hvad betyder oxidation?
1. Elektronoverførsel: Oxidation er en elektrokemisk reaktion, der involverer overførsel af elektroner mellem arter. Når et stof gennemgår oxidation, mister det elektroner, hvilket resulterer i en stigning i dets oxidationstilstand.
2. Oxiderede arter: Stoffet, der undergår oxidation, omtales som den "oxiderede art" eller "reduktionsmiddel". Det donerer elektroner til et andet stof, hvilket forårsager dets egen oxidation.
3. Oxidationsmiddel: Stoffet, der accepterer elektronerne fra den oxiderede art, er kendt som "oxidationsmidlet" eller "oxidanten". Det gennemgår reduktion i processen.
4. Ændring i oxidationsnummer: Oxidation fører generelt til en stigning i oxidationstallet for de oxiderede arter. Oxidationstallet repræsenterer ladningen et atom ville have, hvis alle bindinger til andre atomer var rent ioniske.
5. Eksempler på oxidation:
- Forbrænding: Når et stof brænder i nærværelse af ilt, undergår det en oxidation. For eksempel producerer afbrænding af metan (CH4) med oxygen (O2) kuldioxid (CO2) og vand (H2O).
- Rustning af jern: Jern udsat for ilt og fugt undergår oxidation og danner jernoxid, almindeligvis kendt som rust.
Overordnet set er oxidation en grundlæggende kemisk proces, der driver mange reaktioner i naturen og industrien. Det spiller en afgørende rolle i energiproduktion, metallurgi, fødevarekonservering og forskellige andre processer, hvor stoffer interagerer med ilt.
Sidste artikelHvad er de generelle klasser af kolloider?
Næste artikelEr gæropløsning reversibel eller irreversibel?
 Varme artikler
Varme artikler
-
 Tagrender vrimler med et iøjnefaldende livDiatomer og Paris tagrender. Kredit:© Pascal Jean Lopez / BOREA Biology of Aquatic Organisms and Ecosystems Research Unit (CNRS / MNHN / IRD / UPMC / University of Caen / Université des Antilles).
Tagrender vrimler med et iøjnefaldende livDiatomer og Paris tagrender. Kredit:© Pascal Jean Lopez / BOREA Biology of Aquatic Organisms and Ecosystems Research Unit (CNRS / MNHN / IRD / UPMC / University of Caen / Université des Antilles). -
 Undersøgelse af klimaændringer af tilbagegang i havskildpadder i læder giver ikke svarHavskildpadde i læder. Kredit:Public Domain (Phys.org) – Et team af forskere med Monash University i Australien og West Indies Marine Animal Research and Conservation Service har fundet ud af, at
Undersøgelse af klimaændringer af tilbagegang i havskildpadder i læder giver ikke svarHavskildpadde i læder. Kredit:Public Domain (Phys.org) – Et team af forskere med Monash University i Australien og West Indies Marine Animal Research and Conservation Service har fundet ud af, at -
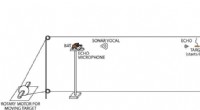 Neurale optagelser af vilde flagermus afslører enestående organisering af mellemhjerneregionen til…Flagermusen trænes til at forblive stationær på en platform og spore et bevægeligt mål. Målet (melorme) er bundet til en løkke af fiskesnøre forbundet til en roterende motor, giver os mulighed for at
Neurale optagelser af vilde flagermus afslører enestående organisering af mellemhjerneregionen til…Flagermusen trænes til at forblive stationær på en platform og spore et bevægeligt mål. Målet (melorme) er bundet til en løkke af fiskesnøre forbundet til en roterende motor, giver os mulighed for at -
 Forskere arbejder mod reversibel slags genredigeringI denne 1. dec. 2015 filbillede, Feng Zhang fra Broad Institute of MIT deltager i en paneldebat på National Summit of Sciences internationale topmøde om sikkerhed og etik ved menneskelig genredigering
Forskere arbejder mod reversibel slags genredigeringI denne 1. dec. 2015 filbillede, Feng Zhang fra Broad Institute of MIT deltager i en paneldebat på National Summit of Sciences internationale topmøde om sikkerhed og etik ved menneskelig genredigering
- Bay Area metan-emissioner kan være det dobbelte af, hvad vi troede
- Digitale færdigheder påvirker børns læringsresultater positivt
- Fra kaos til orden:Hvordan myrer optimerer fødesøgning
- Kemi som byggesten for videnskabelige læsefærdigheder?
- Svirrer støvdjævle rundt om Curiosity-roveren?
- Dyrkere er i klem nu, men jordbærsabotage kan meget vel ende med at hjælpe industrien


