Nyt lægemiddel kunne forhindre invaliderende bivirkning af kræftbehandling

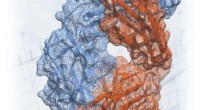
Pladsfyldende struktur skildring af GC4419 baseret på røntgenkrystalstrukturbestemmelse. Kredit:Dennis Riley
Omkring 50, 000 mennesker i USA diagnosticeres årligt med hoved, nakke, kræft i næsen og munden. De fleste behandles med stråling, og af dem, 70-80 procent udvikler en smertefuld og invaliderende bivirkning kaldet alvorlig oral mucositis (SOM). Mens nogle lægemidler er tilgængelige til behandling af SOM, når den udvikler sig, ingen kan forhindre det. Men i dag, forskere rapporterer om et nyt lægemiddel, kaldet GC4419, det ser ud til at gøre netop det. Selvom det stadig er i kliniske forsøg, det er allerede blevet udpeget af U.S. Food and Drug Administration som en "gennembrudsterapi".
Forskerne vil præsentere deres resultater i dag på det 256. nationale møde og udstilling af American Chemical Society (ACS).
"Det er spændende at offentligt rapportere om strukturen og syntesen af GC4419 for første gang, "siger Dennis P. Riley, Ph.d., leder af undersøgelsen. "Vi mener, at GC4419 har potentiale til at imødekomme et vigtigt uopfyldt medicinsk behov i behandlingen af kræftpatienter, der gennemgår strålebehandling, og vi ser frem til at starte et fase 3 -forsøg med GC4419 i kræftpatienter med hoved og hals i år. "
Oral mucositis (OM) er en smertefuld og problematisk komplikation under kræftbehandling, især strålebehandling, som nedbryder epitelcellerne, der forer munden. Patienter, der lider af OM, oplever alvorlige smerter, betændelse, sårdannelse og blødning. De fleste patienter, der får kemoradioterapi, udvikler SOM, som defineret af Verdenssundhedsorganisationen som klasse 3 eller 4 i OM. I de mest alvorlige tilfælde, patienter kan ikke sluge eller indtage væsker eller fast mad, ofte fører til brug af fodringsrør og narkotiske analgetika. Patienter er også modtagelige for infektioner, der kan føre til hospitalsindlæggelse.
Strålebehandling skaber forhøjede superoxidradikale niveauer, som menes at være ansvarlige for de fleste bivirkninger forbundet med denne behandling, herunder OM. "Det syntetiske enzym, vi designede og gjorde, efterligner funktionen af den naturligt forekommende superoxiddismutase, et enzym, der omdanner superoxid til molekylært oxygen og hydrogenperoxid, "siger Riley, der er hos Galera Therapeutics. "Hydrogenperoxid er meget giftigt for kræftceller, men ikke for normale celler. Således Vi skaber to muligheder for at forbedre strålebehandling:at reducere toksicitet for normale celler og samtidig øge toksiciteten for de kræftfremkaldende. "
Design og fremstilling af den syntetiske superoxiddismutase var kompleks, og Rileys team forsøgte mange variationer af syntetiske enzymefterligninger, inden de slog sig ned på GC4419. Forskningen begyndte for årtier siden, da Riley arbejdede hos Monsanto/Searle. Molekylerne, som hans team arbejdede med, havde fire kirale carboncentre, hvilket betød, at der var et meget stort antal potentielle efterligninger.
"Vi var nødt til at finde ud af, hvilken isomer der ville fungere bedst og være den mest 'narkotika, '"rapporterer han." Vores nuværende syntese indebærer at bruge en skabelon til at lave det 15-ledede makrocyliske ringkompleks i et enkelt GMP [Good Manufacturing Practice] -trin. Det bruger pyridin-2, 6- dicarboxyaldehyd, mangan (II) chlorid og et lineært tetramin syntetiseret fra S, S-1, 2 diaminocyclohexan. Det er en elegant enkel 'one-pot' syntese, der giver det ønskede molekyle med mere end 99,5 procent kemisk renhed. "
GC4419 afsluttede med succes fase 1 og 2 kliniske forsøg, viser sikkerhed og effektivitet til forebyggelse af SOM hos kræftpatienter i hoved og hals, der gennemgår strålebehandling. Hvis yderligere kliniske forsøg lykkes, og GC4419 får FDA -godkendelse, Riley siger, "der er ingen grund til, at det ikke kunne bruges til at forhindre bivirkninger fra strålebehandling af andre kræftformer. Du kan tænke på kræft i bugspytkirtlen, for eksempel, hvor du måske vil bruge højdosisstråling til lokalt fremskreden sygdom, men bugspytkirtlen er for tæt på andre organer, der ikke kan håndtere bivirkninger af stråling. Vi studerer i øjeblikket GC4419s antitumor-effekt i et klinisk fase 1/2 forsøg med kræft i bugspytkirtlen på MD Anderson Cancer Center. Hvis det lykkes, dette lægemiddel har potentiale til at ændre styringen af strålebehandling, da 70 procent af alle solide tumorer behandles med stråling. "
Der holdes et pressemøde om dette emne mandag d. 20. august kl. kl. 13.30 Østlig tid i Boston Convention &Exhibition Center. Journalister kan tjekke ind på pressecentret, Værelse 102 A, eller se live på YouTube http://bit.ly/ACSLive_Boston2018. For at stille spørgsmål online, log ind med en Google -konto.
Sidste artikelSpyt kan påvirke smagspræferencer
Næste artikelHvordan en manetformet struktur lindrer trykket i dine celler
 Varme artikler
Varme artikler
-
 At lave strukturelle ændringer af antistof har potentiale til at reducere cancertumorerMolekylær struktur af Frizzled-signalmolekylet som genkendt af et antistof giver tegningerne til kræftterapeutisk finjustering. Kredit:Canadian Light Source Vejledt af blueprints produceret ved de
At lave strukturelle ændringer af antistof har potentiale til at reducere cancertumorerMolekylær struktur af Frizzled-signalmolekylet som genkendt af et antistof giver tegningerne til kræftterapeutisk finjustering. Kredit:Canadian Light Source Vejledt af blueprints produceret ved de -
 Forskere rapporterer kraftig ionoverførsel i ladet vdW-klynge for første gangSammenfaldskortet viser tidspunktet for flyvninger mellem det første og det andet fragmention, der ankommer til detektoren. Kredit:IMP Siden opdagelsen af den dobbelte helixform af DNA og hypote
Forskere rapporterer kraftig ionoverførsel i ladet vdW-klynge for første gangSammenfaldskortet viser tidspunktet for flyvninger mellem det første og det andet fragmention, der ankommer til detektoren. Kredit:IMP Siden opdagelsen af den dobbelte helixform af DNA og hypote -
 Fingeraftryks-narkotest virker på levende og afdødeKredit:CC0 Public Domain En revolutionerende lægemiddeltest udviklet fra forskning udført ved University of East Anglia kan påvise fire klasser af lægemidler i spor af sved fundet i et fingeraftry
Fingeraftryks-narkotest virker på levende og afdødeKredit:CC0 Public Domain En revolutionerende lægemiddeltest udviklet fra forskning udført ved University of East Anglia kan påvise fire klasser af lægemidler i spor af sved fundet i et fingeraftry -
 Forskere ved ESS, Svensk vandforskning, ORNL bruger VISION til at se på almindelige forurenende sto…Brug af neutronspredning, Monika Hartl fra European Spallation Source studerer, hvordan vandfiltre interagerer med forurenende stoffer for at optimere filterdesign og forbedre vandbehandlingsmetoder.
Forskere ved ESS, Svensk vandforskning, ORNL bruger VISION til at se på almindelige forurenende sto…Brug af neutronspredning, Monika Hartl fra European Spallation Source studerer, hvordan vandfiltre interagerer med forurenende stoffer for at optimere filterdesign og forbedre vandbehandlingsmetoder.
- Komet bryder op på flugt af Jorden, fanget af Slooh-medlemmer
- Hvordan vil det offentlige rum ændre sig som følge af COVID-19-pandemien?
- Nyt kvantefænomen hjælper med at forstå grundlæggende grænser for grafenelektronik
- Cassini sender de første billeder fra en ny bane
- Evaluering af aktiv trykstyring af inducerede jordskælv
- Klimaet ændrer sig hurtigere end frygtet, men hvorfor er vi overraskede?


