Forskellen mellem to isotoper af et grundstof?
For eksempel har kulstof tre naturligt forekommende isotoper:kulstof-12, kulstof-13 og kulstof-14. Alle tre isotoper af kulstof har seks protoner, men kulstof-12 har seks neutroner, kulstof-13 har syv neutroner, og kulstof-14 har otte neutroner.
De forskellige isotoper af et grundstof har forskellige fysiske og kemiske egenskaber. For eksempel er kulstof-12 og kulstof-13 begge stabile isotoper, men kulstof-14 er en radioaktiv isotop med en halveringstid på 5.730 år. Det betyder, at kulstof-14 konstant henfalder til nitrogen-14.
De forskellige isotoper af et grundstof kan bruges til en række forskellige formål. For eksempel bruges kulstof-14 til radiocarbondatering, som er en metode til at bestemme organiske materialers alder. Carbon-13 bruges i nuklear magnetisk resonans (NMR) spektroskopi, som er en teknik til at studere strukturen af molekyler.
Samlet set er isotoper vigtige, fordi de bidrager til mangfoldigheden af elementer og giver mulighed for en række forskellige anvendelser inden for videnskab og teknologi.
Sidste artikelHvad er forskellen i atomstruktur mellem to isotoper af klor?
Næste artikelHvor sker gasudveksling af kuldioxid og ilt?
 Varme artikler
Varme artikler
-
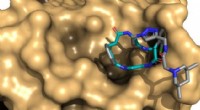 At lære af naturens gavmildhed:Nye biblioteker til lægemiddelopdagelseKunstnerisk skildring af en makrocyklus, der binder til et målprotein. Kredit:Billede:Universitetet i Basel, Basilius Sauter/CC BY-SA 3.0 Naturlige produkter, eller deres nære derivater, lave nogl
At lære af naturens gavmildhed:Nye biblioteker til lægemiddelopdagelseKunstnerisk skildring af en makrocyklus, der binder til et målprotein. Kredit:Billede:Universitetet i Basel, Basilius Sauter/CC BY-SA 3.0 Naturlige produkter, eller deres nære derivater, lave nogl -
 Grønt protein uden smag af kostaldKredit:Miriam Meister Forskere fra DTU Fødevarer har udviklet en teknik til at udvinde protein fra grøn biomasse uden uønsket bismag. Køer kan lide græs for at smage som græs. Imidlertid, hvis fo
Grønt protein uden smag af kostaldKredit:Miriam Meister Forskere fra DTU Fødevarer har udviklet en teknik til at udvinde protein fra grøn biomasse uden uønsket bismag. Køer kan lide græs for at smage som græs. Imidlertid, hvis fo -
 Bioluminescerende orm viste sig at have jern supermagterPergamentrørorm fanget i marken. Kredit:Dr. Evelien De Meulenaere, Scripps Institution of Oceanography ved UC San Diego. Forskere ved Scripps Institution of Oceanography ved University of Californ
Bioluminescerende orm viste sig at have jern supermagterPergamentrørorm fanget i marken. Kredit:Dr. Evelien De Meulenaere, Scripps Institution of Oceanography ved UC San Diego. Forskere ved Scripps Institution of Oceanography ved University of Californ -
 Brækker rumaffald nogensinde naturligt ned? (video)Kan du huske, da Elon Musk sendte en bil ud i rummet? Den bil driver ikke bare fredeligt gennem et vakuum – den suser rundt om solen med 63.592 miles i timen og bliver bombarderet af solstråling. Det
Brækker rumaffald nogensinde naturligt ned? (video)Kan du huske, da Elon Musk sendte en bil ud i rummet? Den bil driver ikke bare fredeligt gennem et vakuum – den suser rundt om solen med 63.592 miles i timen og bliver bombarderet af solstråling. Det
- Kina forbereder sig på at opsende landets første lastrumfartøj
- Digitale trusler formerer sig forud for valget i USA i 2020
- Kulafhængigt Polen til at kompensere industrien for kulstofomkostninger
- Et billede er 1000 ord værd, men hvor mange følelser?
- Virksomheder sporer i stigende grad øjenbevægelser – men er det etisk?
- Smoky Sydney starter nytårsfester med fyrværkeri


