Hvad ville der ske, hvis kobbersulfat fordampede?
1. Vandfordampning: Kobbersulfat findes normalt som et hydrat, hvilket betyder, at det har vandmolekyler bundet til det. Når de opvarmes, fordamper vandmolekylerne først, hvilket efterlader vandfri kobbersulfat (CUSO4).
2. Vandfri kobbersulfat: Den vandfri form er et hvidt pulver. Det er meget hygroskopisk, hvilket betyder, at det let absorberer fugt fra luften og vender tilbage til den hydratiserede form (blå krystaller).
3. Nedbrydning ved højere temperaturer: Hvis temperaturen øges yderligere, begynder vandfri kobbersulfat at nedbrydes. Dette sker ved omkring 650 ° C. Nedbrydningsreaktionen producerer kobberoxid (CuO) og svovltrioxid (SO3) gas.
4. Svovltrioxidadfærd: Svovltrioxidgas vil sandsynligvis reagere med enhver fugt til stede for at danne svovlsyre (H2SO4), en stærk syre. Denne syre kan være ætsende.
Kortfattet:
* Fordampning af vandet: Dette er den første fase.
* Dannelse af vandfri kobbersulfat: Dette er et hvidt pulver.
* nedbrydning ved høje temperaturer: Dette producerer kobberoxid og svovltrioxidgas, som kan danne svovlsyre.
Vigtig note: Håndtering af kobbersulfat og dets nedbrydningsprodukter kræver passende sikkerhedsforanstaltninger, herunder:
* ventilation: Sørg for god ventilation for at undgå indånding af dampe.
* Beskyttelsesudstyr: Bær handsker, beskyttelsesbriller og en laboratoriefrakke for at beskytte din hud og øjne.
* Korrekt bortskaffelse: Bortskaf resterne i henhold til lokale regler.
Sidste artikelHvad hedder Compound Cu2So6?
Næste artikelIoner, der bruges til at etablere et hvilepotentiale?
 Varme artikler
Varme artikler
-
 Forskere omdanner ultrahård pollen til fleksibelt materialeDette pollen-afledte materiale har potentialet til at fungere som en byggesten til design af nye kategorier af miljøvenlige materialer. Afbildet i forgrunden:svampe og papir afledt af pollen. Kredit:N
Forskere omdanner ultrahård pollen til fleksibelt materialeDette pollen-afledte materiale har potentialet til at fungere som en byggesten til design af nye kategorier af miljøvenlige materialer. Afbildet i forgrunden:svampe og papir afledt af pollen. Kredit:N -
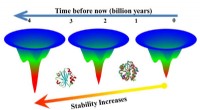 Proteiner, der kan tage varmenGamle proteiner kan tilbyde spor om konstruktionsproteiner til at modstå høje temperaturer, der kræves i industrielle applikationer. Kredit:Rensselaer Polytechnic Institute Gamle proteiner kan giv
Proteiner, der kan tage varmenGamle proteiner kan tilbyde spor om konstruktionsproteiner til at modstå høje temperaturer, der kræves i industrielle applikationer. Kredit:Rensselaer Polytechnic Institute Gamle proteiner kan giv -
 Et revolutionerende materiale til rumfart og neuromorfisk databehandlingVanadium Dioxide chip udviklet på EPFLs NANOLAB. Kredit:EPFL / Jamani Caillet Først kom omskifteren. Derefter transistoren. Nu står en anden innovation for at revolutionere den måde, vi styrer ele
Et revolutionerende materiale til rumfart og neuromorfisk databehandlingVanadium Dioxide chip udviklet på EPFLs NANOLAB. Kredit:EPFL / Jamani Caillet Først kom omskifteren. Derefter transistoren. Nu står en anden innovation for at revolutionere den måde, vi styrer ele -
 Innovativ forarbejdning og emballering for sikker, høj kvalitet, økologiske bærprodukterKredit:Stanislav Samoylik, Shutterstock I løbet af de sidste to årtier, der har været stigende bekymring for de negative virkninger af konventionelt dyrkede produkter på vores sundhed og miljøet.
Innovativ forarbejdning og emballering for sikker, høj kvalitet, økologiske bærprodukterKredit:Stanislav Samoylik, Shutterstock I løbet af de sidste to årtier, der har været stigende bekymring for de negative virkninger af konventionelt dyrkede produkter på vores sundhed og miljøet.
- Ekspertgennemgang afviser planen om at lade havvand strømme ind i New South Wales Murray River
- Fysikere udforsker, hvordan udsving former transportnetværk
- Gamma-stråleteleskoper måler diametre af fjerne stjerner
- T. rex havde et unikt fleksibelt kranium
- Begravet under kolonial beton, Botany Bay er endda blevet berøvet sin botanik
- Skyld ikke Dubais freak regn på skyfrø – stormen var alt for stor til at være menneskeskabt


