Er reaktionshastigheden påvirket af mængdeenzym i miljøet?
* enzymer er katalysatorer: De fremskynder reaktioner uden at blive konsumeret i processen.
* aktive steder: Enzymer har specifikke aktive steder, hvor reaktanter (substrater) binder og gennemgår en kemisk transformation.
* begrænsede aktive steder: Antallet af aktive steder, der er tilgængelige på enzymmolekyler, er begrænset.
* mætning: Når substratkoncentrationen stiger, øges reaktionshastigheden, indtil alle aktive steder er besat. På dette tidspunkt er enzymet mættet, og tilsætning af mere underlag øger ikke reaktionshastigheden yderligere.
Forholdet:
* lav enzymkoncentration: Med en lav enzymkoncentration er der færre aktive steder tilgængelige, så reaktionshastigheden vil være langsommere.
* Høj enzymkoncentration: Med en højere enzymkoncentration er der mere aktive steder tilgængelige, så reaktionshastigheden vil være hurtigere (indtil enzymet er mættet).
Nøgle takeaways:
* Forøget enzymkoncentration =øget reaktionshastighed (indtil mætning)
* Nedsat enzymkoncentration =nedsat reaktionshastighed
Tænk på det sådan: Forestil dig en travl restaurant med kun et par kokke. Hvis du tilføjer flere kokke (enzymer), kan restauranten tjene flere mennesker (reaktanter) hurtigere. Selv med flere kokke er der imidlertid en grænse for, hvor hurtigt de kan arbejde. Når kokke alle er besat, får tilføjelsen af flere kunder ikke restauranten til at køre hurtigere.
 Varme artikler
Varme artikler
-
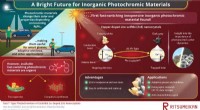 Kobber-doteret zinksulfid ændrer farve reversibelt, når det er belyst og kan bruges i smarte adapt…Forskere har opdaget hurtigt skiftende fotokromisme i et billigt uorganisk materiale:kobber-doterede zinksulfid nanokrystaller. Deres resultater baner vejen for et væld af potentielle applikationer li
Kobber-doteret zinksulfid ændrer farve reversibelt, når det er belyst og kan bruges i smarte adapt…Forskere har opdaget hurtigt skiftende fotokromisme i et billigt uorganisk materiale:kobber-doterede zinksulfid nanokrystaller. Deres resultater baner vejen for et væld af potentielle applikationer li -
 Ny protonstarter til optogenetikKredit:MIPT Forskere har undersøgt et protein, der finder anvendelse i optogenetik og kan bruges til at kontrollere muskler og neuronale celler. Papiret om det lysfølsomme NsXeRprotein fra xenorho
Ny protonstarter til optogenetikKredit:MIPT Forskere har undersøgt et protein, der finder anvendelse i optogenetik og kan bruges til at kontrollere muskler og neuronale celler. Papiret om det lysfølsomme NsXeRprotein fra xenorho -
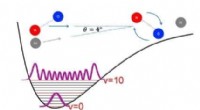 At skubbe studiet af ikke-kovalente intermolekylære interaktioner ind i et nyt områdeFigur af en kollision mellem et stærkt vibrerende NO-molekyle og et argonatom ved en lav kollisionsvinkel, får NO-molekylet til at rotere. Kredit:Hollandsk Organisation for Videnskabelig Forskning (NW
At skubbe studiet af ikke-kovalente intermolekylære interaktioner ind i et nyt områdeFigur af en kollision mellem et stærkt vibrerende NO-molekyle og et argonatom ved en lav kollisionsvinkel, får NO-molekylet til at rotere. Kredit:Hollandsk Organisation for Videnskabelig Forskning (NW -
 På ny bekræfter værdien af internationale samarbejderKredit:CC0 Public Domain Videnskabeligt samarbejde over hele kloden er en vigtig del af moderne forskning. Imidlertid, politiske og økonomiske stridigheder mellem regeringer, såsom de nuværende sp
På ny bekræfter værdien af internationale samarbejderKredit:CC0 Public Domain Videnskabeligt samarbejde over hele kloden er en vigtig del af moderne forskning. Imidlertid, politiske og økonomiske stridigheder mellem regeringer, såsom de nuværende sp
- Hvad er de store huller, der dækker kviksølv?
- Boston Harbor -oprydning var økonomisk forsvarlig, finder en ny undersøgelse
- American Express køber restaurantreservationstjenesten Resy
- Den pandemiske nedlukning fører til renere byluft i hele Canada, papir afslører
- I et fjernt stjernesystem ser JWST enden på planetdannelsen
- Rapport om tilbud af behandlere til børn og unge med særlige pædagogiske behov og handicap


