Hvad er Arrhenius-syrer?
Ifølge Arrhenius-teorien er syrer stoffer, der dissocierer i vand for at producere H+-ioner. Disse H+ ioner er ansvarlige for opløsningens sure egenskaber. Jo højere koncentrationen af H+ ioner i en opløsning er, jo stærkere er syren.
Nogle almindelige eksempler på Arrhenius-syrer omfatter:
- Saltsyre (HCl)
- Svovlsyre (H2SO4)
- Salpetersyre (HNO3)
- Eddikesyre (CH3COOH)
Arrhenius-syrer er typisk ætsende og kan reagere med metaller for at producere brintgas. De kan også reagere med baser for at producere salte og vand.
 Varme artikler
Varme artikler
-
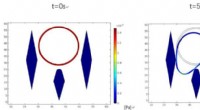 Små filtre hjælper med at opdage kræftblodcellerSimuleringer, der viser cancerøse myelomceller, også kendt som cCPCer, sidde fast mellem mikrosøjler i en ny filterenhed, beskrevet i Biomicrofluidics. Blå kontur er cCPCen, og væsken strømmer fra top
Små filtre hjælper med at opdage kræftblodcellerSimuleringer, der viser cancerøse myelomceller, også kendt som cCPCer, sidde fast mellem mikrosøjler i en ny filterenhed, beskrevet i Biomicrofluidics. Blå kontur er cCPCen, og væsken strømmer fra top -
 En ny metode til at udskrive spejle af variabel størrelse med en reflektionsevne på mere end 99 %Farvet spejllag printet på en folie. Inkjet-udskrivning giver mulighed for strukturering, således at store logoer også kan udskrives. Kredit:Qihao Jin, KIT Dielektriske spejle, også kaldet Bragg-sp
En ny metode til at udskrive spejle af variabel størrelse med en reflektionsevne på mere end 99 %Farvet spejllag printet på en folie. Inkjet-udskrivning giver mulighed for strukturering, således at store logoer også kan udskrives. Kredit:Qihao Jin, KIT Dielektriske spejle, også kaldet Bragg-sp -
 Udforskning af den neurologiske påvirkning af luftforureningKredit:CC0 Public Domain Luftforurening er blevet en kendsgerning i det moderne liv, med et flertal af den globale befolkning, der står over for kronisk eksponering. Selvom virkningen af at indå
Udforskning af den neurologiske påvirkning af luftforureningKredit:CC0 Public Domain Luftforurening er blevet en kendsgerning i det moderne liv, med et flertal af den globale befolkning, der står over for kronisk eksponering. Selvom virkningen af at indå -
 Verdens ældste ost fundet i egyptisk gravKredit:American Chemical Society Lagring forbedrer normalt smagen af ost, men det er ikke derfor, at en meget gammel ost, der blev opdaget i en egyptisk grav, gør opmærksom. I stedet, det menes
Verdens ældste ost fundet i egyptisk gravKredit:American Chemical Society Lagring forbedrer normalt smagen af ost, men det er ikke derfor, at en meget gammel ost, der blev opdaget i en egyptisk grav, gør opmærksom. I stedet, det menes
- Grønlands landskabshistorie bevaret under indlandsisen
- Bots målretter og forfølger faktisk individuelle påvirkere
- Forskere foreslår den optimale måde at producere biobrændstoffer på
- Lockheed Martin starter næste Orion-rumfartøj for første gang
- At spille på gode følelser:Når eudaimonic sociale medier går dårligt
- Fem ting EU gør for miljøet


