
Essencer

Kemi
- Fødevareemballage i plast kan indeholde skadelige kemikalier, der påvirker hormoner og stofskifte, finder forskere
- Hvilket materiale har formbarhed?
- Syreeffekt på havet?
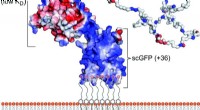
- Kædelængde bestemmer molekylær farve, muliggør farvejustering til medicinsk billeddannelse
- Hvis 0,1 koncentration af HCL, hvor meget pH?

- Hvad er det bedste eksempel på en prokaryot celle?
- Bakterieceller reproducerer sig aseksuelt af hvad?
- Eksempler på seksuel reproduktion:En guide til kongerige
- Hvad er mængden af gener i en menneskelig celle?
- Thailand gemmer på store tal, når det kommer til sine fiskefangster i de tilstødende farvande


 Kemi
Kemi
 Astronomi
Astronomi
 Energi
Energi
 Andet
Andet
